Узмите у обзир следећу хемијску равнотежу при константној температури:
3 сата2 (г) + Н.2 (г) НХ 2 НХ3 (г)
Према Гаи-Луссац-у, удео запремине гасовитих учесника у реакцији једнак је односу одговарајућих стехиометријских коефицијената. Једноставно речено, можемо рећи да је број молекула присутних у реактантима и производима једнак коефицијентима у једначини.
У случају горе, у реагенсима имамо 4 молекула, а у производима 2 молекула, што значи да је запремина реагенса већа, а количина производа мања.
Ако повећамо притисак у овом систему, равнотежа ће се померити ка мањој запремини да би смањила овај притисак. У случају реакције коју разматрамо, истискивање ће бити у директном смеру стварања производа (НХ3 (г)).
Међутим, ако смањимо притисак, реакција ће се кретати ка највећој запремини, која је супротног смера, стварања реактаната (3 Х2 (г) + Н.2 (г)).
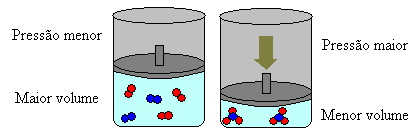
То се дешава према принципу Ле Цхателиер-а, који каже да је сваки поремећај (попут смањења или повећања притиска) изазван у систему у равнотежи учиниће да се креће у смеру који минимизира овај поремећај, прилагођавајући се новом равнотежа.
Укратко, у случају утицаја промене притиска на хемијску равнотежу можемо рећи следеће:
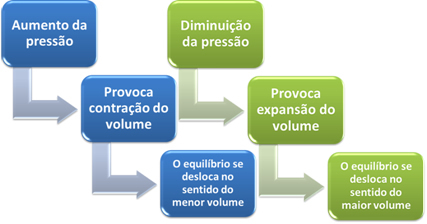
У случају реакција у којима је запремина реактаната једнака запремини производа, хемијска равнотежа се не мења.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm


