Када храну кувамо у својим домовима, користимо сагоревање гаса за кување. Једна од ствари коју можемо видети у пламену који настаје сагоревањем овог гаса је да је његова боја обично врло светло плава. Међутим, у већини реакција сагоревања, попут горења свеће, пламен је жут.

Тада се поставља питање:
„Ако је сваки пожар резултат реакције сагоревања, зашто неки пламенови имају различите боје?“
Да бисмо разумели како се то дешава, морамо да разумемо шта је реакција сагоревања и које супстанце су присутне у свакој од поменутих реакција.
Реакција сагоревања се јавља када оксиданс (гасовити материјал који садржи кисеоник) троши гориво (оксидирајући материјал) за генерисање топлотне енергије (топлоте).
Још једна важна тачка коју морамо знати о реакцијама сагоревања је да се оне могу одвијати у а потпун или непотпун. Ако има довољно кисеоника за трошење горива, реакција ће бити потпуна и произвешће угљен-диоксид (ЦО2) и воде (Х.2О). У супротном, сагоревање ће бити делимично, непотпуно, стварајући угљен моноксид (ЦО) и воду; или угљеник (Ц) и вода.
У оба случаја која анализирамо, оксиданс је кисеоник присутан у ваздуху. Међутим, горива су различита. Гас за кување је заправо течни нафтни гас (ТНГ), који је смеша угљоводоника (алкани), а главно гориво је бутан (Ц4Х.10). Дакле, гас за кување чине само молекули алкана три или четири атома угљеника, зато је за његово сагоревање потребно мало кисеоника. Ова реакција се може изразити на следећи начин:
1Ц4Х.10 (г) + 13/2 О.2 (г) → 4 ЦО2 (г) + 5 сати2О.(г), ∆Х <0
У случају свећа, парафин је гориво за реакцију, а састоји се од мешавине алкана са атомима угљеника која крећу се од 20 до 36. Тиме, потребно је много више кисеоника да би се ова реакција одвијала у потпуности. Погледајте пример:
1Ц24Х.50 (с) + 70/2 О.2 (г) → 25 ЦО2 (г) + 25 Х.2О.(г), ∆Х <0
У ваздуху нема довољно кисеоника за спровођење овог потпуног сагоревања, па се оно одвија непотпуно, као што је приказано доле:
1Ц24Х.50 (с) +49/2 О.2 (г) → 24 ЦО(г) + 25 Х.2О.(г), ∆Х <0
1Ц24Х.50 (с) +25/2 О.2 (г) → 24Ц(с) + 25 Х.2О.(г), ∆Х <0
Непотпуне реакције производе мање енергије од потпуног сагоревања. Ово објашњава разлику између боја пламена, јер жути пламен, карактеристичан за непотпуно сагоревање, има нижу енергију. Плави пламен је карактеристичан за потпуно сагоревање, са већом енергијом.
Ово такође објашњава стварање чађи у пламену свеће (слика доле), а то је угљеник који се сматра производом непотпуног сагоревања.
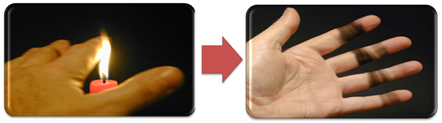
Али зашто је у Бунсеновом горионику могуће добити жути и плави пламен када се гориво не мења?
У случају Бунсеновог горионика, то се постиже регулисањем улаза гаса и ваздуха. Ако је прозор затворен, што узрокује улазак мале количине ваздуха, добијени пламен ће бити жут, јер ће имати мало кисеоника за потпуно сагоревање. Ако је регулација смеше гас-ваздух одговарајућа, добићемо плави пламен.
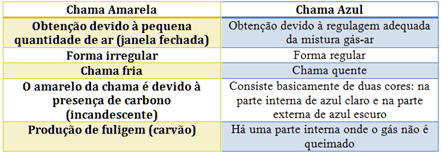
Погледајте карактеристике сваке од њих у доњој табели:
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/combustao-chamas-cores-diferentes.htm
