Материја може проћи две главне врсте трансформација, физичку и хемијску. Физичка трансформација је када се природа материје не мења, односно њен састав. На пример, када смо посекли комад дрвета, оно је претрпело трансформацију, али то је био физички феномен, јер је и даље дрво, његова конституција је иста као на почетку.
С друге стране, хемијска трансформација или појава настаје када се промени природа или састав материје. У овом случају, почетне честице (које могу бити молекули, атоми, јонски кластери, јони итд.) Су попут растављају се и њихови атоми преуређују, састављајући нове молекуле, кластере, атоме, јоне итд., односно нове супстанце. Ово је хемијска реакција.
На пример, замислите да упаљену шибицу приближимо етилном алкохолу. Знамо шта ће се догодити: алкохол ће почети да гори. То значи да је у хемијској реакцији са кисеоником у ваздуху (О2) и промениће његов састав, више није етанол (Ц.2Х.6О), а кисеоник такође више неће имати свој почетни састав, потичући нове супстанце, а то су угљен-диоксид (ЦО2) и воде (Х.2О).

Алкохол у пламену - реакција сагоревања
У хемијским реакцијама се називају почетне супстанце реагенси и крај производи, а реакције су представљене кроз хемијске једначине, који следе следећу општу структуру:
РЕАГЕНТИ → ПРОИЗВОДИ
Узимајући у обзир претходни пример потпуне реакције сагоревања алкохола (етанола), имамо следећу хемијску једначину:
Етанол + гас кисеоника → Угљен-диоксид + вода
Ова хемијска реакција је у наставку представљена помоћу атома према Далтоновом моделу, у облику једноставних сфера:
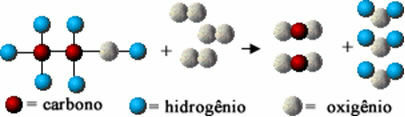
Моделни приказ реакције сагоревања етанола
Приметите да су почетне везе између атома биле прекинуте и да су створили нове везе и појавиле су се нове супстанце.
Дакле, хемијске једначине су написане помоћу формула и симбола који најбоље представљају горњу шему. У разматраном случају (реакција сагоревања етанола) имамо да је хемијска једначина изражена на следећи начин:
Ц2Х.5ох(?) + 3 О.2 (г) → 2 ЦО2 (г) + 3 Х.2О.(в)
Постоје неки визуелни фактори који указују на постојање хемијске реакције, а то су:
* Отпуштање гаса;
* Промена боје;
* Стварање талога;
* Изглед пламена или сјаја.
Важни процеси који се дешавају у нашем телу, у природи и у индустријама, попут производње лекова и индустријализоване хране, су хемијске реакције. Због тога су изузетно важни за настанак и одржавање живота.
Постоји неколико врста хемијских реакција, које се могу класификовати према различитим критеријумима, али главне врсте које се проучавају у хемији су:
1. Неорганске реакције: Обично се класификују према броју формираних супстанци, броју реагенса и присуству или одсуству једноставних и сложених супстанци. Постоје четири главне врсте неорганских реакција:
1.1. Реакције синтезе или адиције;
1.2. Реакција распадања или анализе;
1.3. Једноставна замена, померање или редокс реакција;
1.4. Реакција двоструке размене или метатезе;
2. Органске реакције: То су они који укључују угљенична једињења. Генерално се класификују у три главне врсте:
2.1. Реакције сабирања;
2.2. Реакције замене;
2.3. Реакције елиминације.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-reacao-quimica.htm
