ти нитро једињења карактерише присуство следеће функционалне групе:
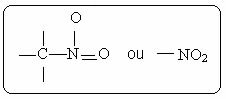
Међу његовим дериватима, најпознатији је нитробензол, који је жута, токсична, у води нерастворљива, густа течност која се користи као растварач за органске супстанце.
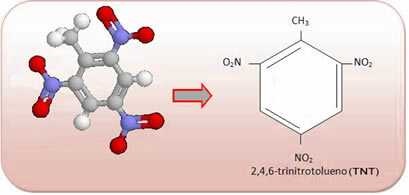
Ова једињења су веома реактивна, па се широко користе као експлозиви. Неки добро познати примери су 2-метил-1,3,5-тринитробензен или 2,4,6-тринитротолуен (ТНТ), или 2,4,6-динитротолуен (ДНГ) и тринитроглицерина (ТНГ), који се, осим што је експлозив, користи и као коронарни вазодилататор у случају ризика од инфаркт.
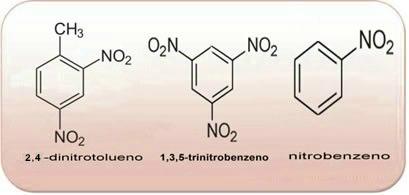
Сва горња једињења су ароматична, што је већа количина НО2 у својим молекулима, то ће бити експлозивније. Њихови препарати и својства су веома различити од оних алифатских нитро једињења. Нитроалкани су безбојне, поларне течности, такође нерастворљиве у води и користе се у органским синтезама, као интермедијери и као растварачи.
Номенклатура нитроједињења следи правило у наставку, које је установила Међународна унија чисте и примењене хемије (ИУПАЦ):

Дакле, имамо следећа имена за структуре нитроједињења у наставку:
Х3Ц__АТ ТХЕ2: нитрометан
Х3Ц__ЦХ2__АТ ТХЕ2: нитроетан
Х3Ц__ЦХ2__ ЦХ2__АТ ТХЕ2: 1- нитропропан
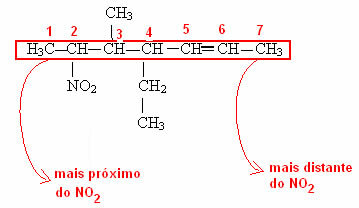
Имајте на уму да је у последњем примеру било неопходно нумерисати одакле долази функционална група угљеничног ланца. Ово нумерисање се увек врши почевши од најближег краја функционалне групе. Погледајте како се то ради у примеру испод:
Аутор: Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил школа - https://brasilescola.uol.com.br/quimica/nitrocompostos.htm
