ПХ одговара хидрогеном потенцијалу раствора. Одређује се концентрацијом јона водоника (Х+) и служи за мерење степена киселости, неутралности или алкалности датог раствора.
Поред пХ, постоји и друга величина која одређује киселост и базност воденог система: пОХ (хидроксилиони потенцијал). Ова скала има исту функцију као пХ, мада се мање користи.
пХ скала
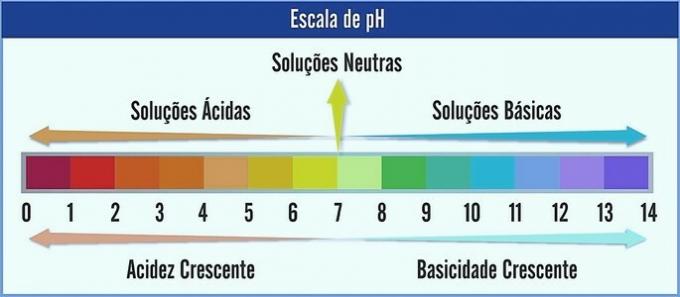
ПХ је представљен на скали од 0 до 14. Мери киселост и базност раствора.
Стога пХ 7 представља неутрални раствор (нпр. Чиста вода). Они пре њега сматрају се киселим растворима (кисели пХ), а они после 7 су основни раствори (алкални пХ).
Овим запажањем, киселински карактер се повећава с десна на лево. Основни лик, слева надесно. Имајте на уму да што је нижа вредност пХ, раствор ће бити киселији.
Сазнајте више на:
- Пуферски раствор
- Титрација
- Реакција неутрализације
Примери
Ацид Солутионс
| Решење | пХ |
|---|---|
| Гастрични сок | 2,0 |
| Сок од лимуна | 2,2 |
| Сирће | 3,0 |
| Кафа | 5,0 |
| Кравље млеко | 6,4 |
Основна решења
| Решење | пХ |
|---|---|
| људска крв | 7,35 |
| Морска вода | 7,4 |
| Натријум бикарбоната | 8,4 |
| Млеко магнезијума | 10,5 |
| Блеацх | 12,5 |
Како израчунати пХ?
Дански хемичар Сорен Соренсен (1868-1939) 1909. године предложио је да киселост раствора, мерено концентрацијама Х јона+, трансформисао је своје вредности користећи логаритме да би се олакшало разумевање.
На температури од 25 ° Ц, јонски производ воде је једнак 10–14 мол2/ Л2.
Примењујући кологаритам у изразу, морамо:
Кроз овај израз можемо одузимањем добити одговарајућу вредност са једне скале на другу.
Како измерити пХ?
Контрола пХ вредности није важна само у научне сврхе, већ и у свакодневном животу.
Треба проверити пХ базена, као и пХ акваријума, па чак и пХ тла, како би се омогућиле одређене врсте усева.
Испод су наведени главни начини мерења пХ.
киселинско-базни индикатор
За мерење пХ раствора користе се такозвани индикатори киселинске базе. Они су супстанце које мењају боју указујући на карактер раствора. Најкоришћенији индикатори су: лакмус и фенолфталеин.

Педометар
Поред индикатора, пХ раствора може се мерити помоћу инструмента који се назива пеагометар. Овај електронски уређај мери електричну проводљивост раствора и претвара га у скалу пХ вредности.

Вежбе пријемног испита са повратним информацијама
1. (Енем / 2014) Истраживач схвата да је етикета једне од наочара у којој држи концентрат дигестивних ензима нечитка. Не зна који ензим чаша садржи, али сумња да је то желучана протеаза, која у желуцу делује сварењем протеина.
Знајући да је варење у желуцу кисело, а црево основно, он саставља пет епрувета са храном различито, додајте концентрат ензима у растворе са утврђеним пХ и сачекајте да видите да ли ензим делује у било ком њихов.
Епрувета у којој ензим мора деловати да би указао на исправност хипотезе истраживача је она која садржи:
а) коцка кромпира у раствору са пХ = 9
б) комад меса у раствору са пХ = 5
в) кувано бело јаје у раствору са пХ = 9
г) део јуфке у раствору са пХ = 5
д) лоптица путера у раствору са пХ = 9
Тачна алтернатива: б) комад меса у раствору са пХ = 5.
Протеаза је ензим који пробавља протеине и зато што је желудац, делује у желуцу чији је пХ кисео.
Анализирајући алтернативе, морамо:
а) ПОГРЕШНО. Кромпир је богат угљеним хидратима, а пХ концентрата је основни.
б) ТАЧНО. Месо садржи протеине и ензими могу деловати на њега, а пХ концентрата је кисео, попут желуца.
в) ПОГРЕШНО. ПХ концентрата је основни.
г) ПОГРЕШНО. Тестенине су богате угљеним хидратима.
е) ПОГРЕШНО. ПХ концентрата је основни.
2. (Удесц / 2009) „Кисела киша“ је термин који се односи на падавине из атмосфере кише са више од нормалних количина азотне и сумпорне киселине.
Претходници киселих киша долазе како из природних извора, попут вулкана и пропадајуће вегетације, тако и из процеса индустријске емисије, углавном сумпор диоксида и азотних оксида из сагоревања горива фосили.
ПХ кишнице који се сматра нормалним је 5,5 (због присуства угљене киселине из солубилизације угљен-диоксида). Хемичар који надгледа високоиндустријализовани регион приметио је да је пХ кишнице 4,5.
С обзиром на то да је киселост повезана са концентрацијом Х.3О.+, тачно је рећи да је вода са пХ 4,5 била:
а) двоструко основнији од нормалног.
б) двоструко киселији од нормалног.
в) десет пута основније од нормалног.
г) десет пута киселији од нормалног.
д) сто пута киселији од нормалног.
Тачна алтернатива: г) десет пута киселији од нормалног.
Према изразима пХ = - лог [Х+] и [Х.+] = 10-пХ, Морамо да:
пХ = 5,5
[Х+] = 10-5,5
пХ = 4,5
[Х+] = 10-4,5
Разлика између вредности је: 10- 5,5 - ( - 4,5) = 10 -1
Како је пХ скала логаритамска скала, промена једне јединице једнака је 10 пута киселијем раствору.
3. (УФМГ / 2009) Узмите у обзир одређену количину воде и лимуновог сока, помешаних, садржаних у чаши. Прегледајте ове три изјаве у вези са овим системом:
И. Систем је кисео.
ИИ. ПХ система је већи од 7.
ИИИ. У систему је концентрација Х јона+ је већи од ОХ–.
На основу ове анализе ТАЧНО је тврдити да:
а) тачне су само изјаве И и ИИ.
б) тачне су само изјаве И и ИИИ.
в) тачне су само изјаве ИИ и ИИИ.
г) све три изјаве су тачне.
Тачна алтернатива: б) тачне су само изјаве И и ИИИ.
И. ТАЧНО Лимун садржи лимунску киселину која у раствору ослобађа јоне Х.+ и тако је систем кисео.
ИИ. ПОГРЕШНО. ПХ је мањи од 7, што карактерише кисели систем: што је пХ вредности раствора ближи 0, то је киселији.
ИИИ. ТАЧНО Кисели пХ је резултат високе концентрације јона Х+ у раствору, пошто је пХ = - лог [Х+].
За више питања, уз коментарисану резолуцију, обавезно проверите:Вежбе на пХ и пОХ.