Сулфати су јонска једињења која садрже анион СО42-, који се назива сулфатни анион.
Сумпор је елемент породице 16 или ВИ-А, што значи да у својој валентној љусци има 6 електрона. Према правилу октета, требало би да прими још 2 електрона да би у последњој електронској љусци било 8 електрона и тако био стабилан. Али сумпор пролази кроз проширење октета, јер је елемент смештен у трећем периоду Табеле Периодична, релативно велика, што јој омогућава да прими више од осам електрона око.
Дакле, као што се може видети доле, ниво валенције сумпора се шири и смешта укупно 12 електрона. Али два атома кисеоника још увек нису стабилна, сваки са по седам електрона у валентној љусци, па треба да прими још један електрон за стабилизацију. Из тог разлога је наелектрисање сваког од ова два атома -1, што резултира укупним наелектрисањем аниона од -2:
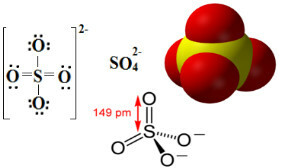
Анион сулфата може потицати из сумпорне киселине (Х2САМО4 (ак)) приказано испод:
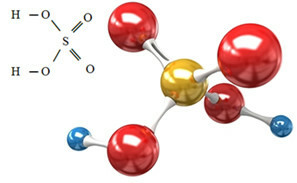
Сумпорна киселина реагује са неком базом, у реакцији неутрализације, формирајући неорганску со, која је наш сулфат, а такође и воду:
Генеричка реакција: Сумпорна киселина + база → Сол (сулфат) + вода
Х.2САМО4 + 2 Цох →Ц2САМО4+ 2 Х.2О.
Погледајте пример испод где се формира калијум сулфат:
Х.2САМО4 + 2 КОХ →К.2САМО4+ 2 Х.2О.
Имајте на уму да се номенклатура сулфата врши једноставно по правилу: сулфат + назив елемента који је везан за њега. Поред тога, формуле за сулфате израђене су разменом наелектрисања сваког јона за индекс елемената, при чему индекс "1" није потребно писати:
Примери:
У+1 САМО42- → У2САМО4→ натријум сулфат
мг+2 САМО42- → МгСО44→ магнезијум сулфат
Ево+2 САМО42- → Случај4→ калцијум сулфат
Ба+2 САМО42- → БАСО4→ баријум сулфат
Ал+3 САМО42- → Ал2(САМО4)3→ алуминијум сулфат
Соли које садрже сулфатни јон су обично растворљиве у води, изузетак су четири: калцијум сулфат (ЦаСО4), стронцијум сулфат (СрСО4), баријум сулфат (БаСО4) и оловног сулфата (ПбСО4). То је зато што постоји велика енергија везивања између ових катиона (Ца2+, господине2+, Ба2+ и Пб2+) и сулфата, јер сви имају наелектрисање +2, а сулфатни анион наелектрисање -2. Дакле, прекидање те везе постаје теже.
Сулфати се налазе у облику кристалних решетки, због привлачења које супротни набоји врше једни на друге, као што је доле приказано у случају бакар сулфата (ЦуСО4):

Сулфати се у природи налазе углавном у облику минерала. Погледајте неке примере:
барит → баријум сулфат;
Гипс → калцијум сулфат;
Целестите → стронцијум сулфат;
англесиУ реду → оловни сулфат;
Глауберите → двоструки калцијум и натријум сулфат: ЦаНа2(САМО4)2;
Калијум стипса (калинит) → хидратисани двоструки калијум алуминијум сулфат: КАл (СО4) 2.11Х2О.
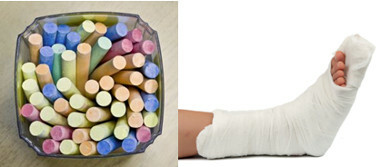
Међу главним сулфатима у свакодневном животу имамо калцијум сулфат, који се у безводном облику (без воде) користи у производњи школске креде. Када је у дихидратном облику, (ЦаСО4 .2х2О), познат је под називом гипс и обилнији је. Загријавањем формира калцијум сулфат хемихидрат (ЦаСО4. ½Х.2О), који је гипс, користи се у ортопедији, зубним калупима, цивилној градњи и бојама.
Друга важна со је смагнезијум сулфат (МгСО44), познат као сгорка ал или Епсомова со, која делује лаксативно и користи се за масажу и опуштајуће купке.
Јеннифер Фогаца
Дипломирао хемију
