Хемијска изомерија је појава која се примећује када две или више органских супстанци имају исту молекулску формулу, али различиту молекуларну структуру и својства.
Хемијске супстанце са овим карактеристикама називају се изомери.
Термин је изведен из грчких речи исо = једнак и пуки = делова, односно једнаких делова.
Постоје различите врсте изомерије:
- равни изомер: Једињења се идентификују помоћу равних структурних формула. Подијељен је на ланчану изомерију, изомерију функције, изомерију положаја, изомерију компензације и изомерију таутомерије.
- свемирски изомер: Молекуларна структура једињења има различите просторне структуре. Подијељен је на геометријску и оптичку изомерију.
равни изомер
У равна изомерија или уставна изомерија, молекуларна структура органских супстанци је равна.
Једињења која показују ову карактеристику називају се равни изомери.
изомер ланца
Ланчана изомерија се дешава када атоми угљеника имају различите ланце и исту хемијску функцију.
Примери:
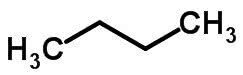
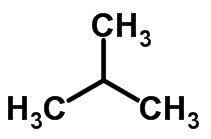
Изомерија функције
Изомерија функције се јавља када два или више једињења имају различите хемијске функције и исту молекулску формулу.
Примери: Овај случај је уобичајен између алдехида и кетона.
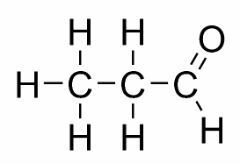
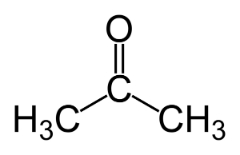
Изомер положаја
Изомерија положаја се јавља када се једињења диференцирају различитим незасићеним, разгранатим или функцијским положајима у ланцу угљеника. У овом случају, изомери имају исту хемијску функцију.
Примери:

офсетинг изомер
Компензациона изомерија или метамеризам се јавља у једињењима са истом хемијском функцијом која се разликују по положају хетероатома.
Примери:

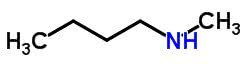
Таутомерија
Таутомеризам или динамичка изомерија могу се сматрати посебним случајем изомеризма функција. У овом случају, један изомер се може променити у други променом положаја елемента у ланцу.
Примери:

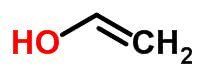
свемирски изомер
ТХЕ свемирска изомерија, која се назива и стереоизомерија, дешава се када два једињења имају исту молекулску формулу и различите структурне формуле.
У овој врсти изомерије, атоми се дистрибуирају на исти начин, али заузимају различите положаје у простору.
геометријски изомер
ТХЕ геометријска изомерија или се цис-транс јавља у незасићеним отвореним ланцима, а такође и у цикличним једињењима. Да би се то урадило, лиганди угљеника морају бити различити.

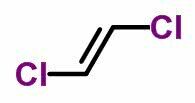
- Када су исти лиганди на истој страни, изомерна номенклатура добија префикс цис.
- Када су исти лиганди на супротним странама, номенклатура добија префикс транс.
ИУПАЦ (Међународна унија чисте и примењене хемије) препоручује да се уместо цис и транс, слова З и Е користе као префикс.
То је зато што је З прво слово немачке речи зусаммен, што значи „заједно“. И то је прво слово немачке речи ентегеген, што значи „супротно“.
оптички изомер
ТХЕ оптичка изомерија показују једињења која су оптички активна. То се дешава када је супстанца узрокована угаоним одступањем у равни поларизоване светлости.
- Када супстанца савије оптичку светлост удесно, она се зове дешњак.
- Када супстанца савије оптичку светлост улево, она се зове леворотари.
Супстанца такође може постојати у два оптички активна облика, декстогира и левогира. У овом случају се зове енантиомер.
Да би једињење угљеника било оптички активно, мора бити хирално. То значи да се њихови лиганди не могу преклапати, будући да су асиметрични.
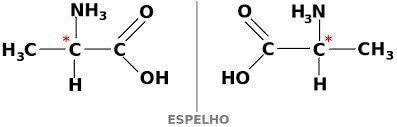
Заузврат, ако једињење има декстрогиру и леворотарни облик у једнаким деловима, они се зову рацемске смеше. Оптичка активност рацемских смеша је неактивна.
Прочитајте такође:
- Угљеник
- Органска хемија
- Молекуларна формула
- структурна формула
Вежбе
1. (Мацкензие 2012) Бројна колона Б, која садржи органска једињења, повезујући их са колоном А, према врсти изомерије коју сваки органски молекул представља.
Колона А.
1. офсетинг изомер
2. геометријски изомер
3. изомер ланца
4. оптички изомер
Колона Б.
() циклопропан
() етокси-етан
() бромо-хлоро-флуоро-метан
() 1,2-дихлоро-етен
Тачан низ бројева у колони Б, од врха до дна, је
а) 2 - 1 - 4 - 3.
б) 3 - 1 - 4 - 2.
в) 1 - 2 - 3 - 4.
г) 3 - 4 - 1 - 2.
е) 4 - 1 - 3 - 2.
Алтернатива б) 3 - 1 - 4 - 2.
2. (Уерј) Изомерија је феномен који се одликује чињеницом да иста молекулска формула представља различите структуре.
Узимајући у обзир равну структурну изомерију за молекуларну формулу Ц.4Х.8, можемо идентификовати изомере следећих врста:
а) ланац и положај
б) ланац и функција
в) функција и компензација
г) положај и накнада
Алтернатива а) низ и положај
3. (ОСЕЦ) Пропанон и изопропенол представљају пример изомерије:
а) од метамерије
б) функције
в) таутомерије
г) цис-тран
д) ланац
Алтернатива ц) таутомерије
Види и ти: Вежбе на равној изомерији


