Супстанце су материјали који имају сва својства добро дефинисана, утврђена и практично константна.
Погледајте три примера:
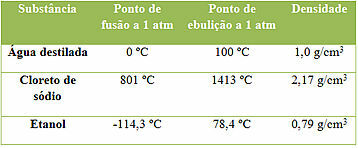
Примери три супстанце и њихова својства
Имајте на уму да су ово три супстанце и да су њихова својства константна када се мере под истим условима температуре и притиска. Али свака има различите вредности својстава, јер ниједна две супстанце немају сва својства потпуно иста. Ово је важно јер се помоћу њих може идентификовати супстанца.
Атоми су најмањи саставни делови материје и они могу остати изоловани, као што се, на пример, догађа у случају гаса хелијума, који се формира од атома хелијума (Хе); али се такође могу везати на разне начине, формирајући молекуле (у случају оних који се везују ковалентно делећи парове електрони) или јонски кластери (који се везују јонском везом, у којима један дефинитивно дарује електроне другом и настају јони који формирају привући).
Тако, супстанце могу настати од атома, молекула или јонских кластера. Вода и етанол настају молекулима, који су Х.
2О и Ц.2Х.5ОХ, док натријум хлорид творе јонски агломерати чија је јединствена формула НаЦ ?.
Вода и сол су примери супстанци
Ови примери показују да се супстанце могу класификовати према групи атома који их чине. Ако су атоми који се спајају да би створили супстанцу истог хемијског елемента, онда имамо а једноставна супстанца. Неки примери су: гас са кисеоником (О.2), водоник гас (Х.2), гвожђе (Фе), гас хелијума (Хе), алуминијум (А?) итд.
С друге стране, ако супстанце настају од атома два или више различитих елемената, као што су вода, етанол и натријум хлорид, тада ће се класификовати као сложена супстанца.
У природи није уобичајено проналазити супстанце у изолованом, чистом облику. Обично се налазе помешани са другим супстанцама. На пример, минерална вода коју пијемо садржи много растворених супстанци, а не само молекуле Х.2О; зато је она Микс, а не супстанца.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-substancia.htm
