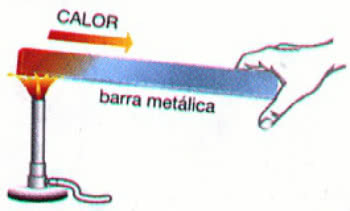
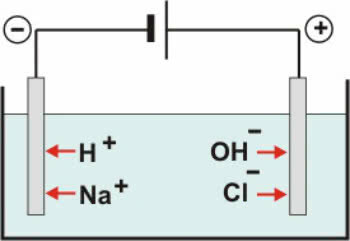
Ендотермне и егзотермне реакције су количине које мере количину топлоте (енергије) апсорбоване и ослобођене током хемијских реакција. Проучава их термохемија.
Која је разлика између њих?
ендотермна реакција је онај у коме постоји апсорпција енергије. У овом процесу се енергија производи и самостално одржава.
Птице и сисари имају способност да одржавају стабилну телесну температуру. Из тог разлога се називају ендотермним животињама, популарно "топлокрвним животињама".
Егзотермна реакција је онај у коме долази до ослобађања енергије. У овом процесу, производња енергије траје само кроз непрекидно снабдевање енергијом.
Промена физичких стања, тим редоследом: гас, течност и чврсто стање, пример је егзотермне реакције. Свака од њих се јавља како се енергија ослобађа, односно када има мање топлоте.
Имајте на уму да када преокренемо овај редослед (чврста, течна и гасна), производи се енергија (више топлоте). У овом случају, реакција је ендотермна.
Свакодневни примери
Телесна масноћа делује као гориво у нашем телу. Она која није изгорела, апсорбује је. Како је ово процес апсорпције, пример је ендотермне реакције.
Када стављамо посуду на ватру за припрему хране, заузврат смо суочени са егзотермним процесом. То је зато што топлота која се ослободи трансформише ову храну тако да се може потрошити.
А шта је енталпија?
енталпија то је енергија која постоји у свим супстанцама и која се мења као резултат ендотермних и егзотермних реакција.
Како енталпију није могуће израчунати, утврђен је прорачун њене варијације.
Дакле, упоређивањем стандардне енталпије (температура од 25 ° Ц под атмосферским притиском од 1атм), било би могуће израчунати варијацију енталпије.
Према Хессов закон, коначна енталпија минус почетна енталпија (ΔХ = Хф - Хи) резултира овим подацима.
Ако ендотермна реакција апсорбује енергију, то значи да је енталпија (крајњег) реактанта нижа од оне (почетног) производа. Стога је промена енталпије позитивна (ΔХ> 0).
Заузврат, ако егзотермна реакција ослобађа енергију, то значи да је енталпија (енергија) реактанта већа од енталпије производа. Стога је варијација енталпије негативна (ΔХ
Прочитајте такође:
- Хемијске реакције
- Хемијска равнотежа
- Сагоревање