Киселине и базе су две међусобно повезане хемијске групе. То су две супстанце од великог значаја и присутне у свакодневном животу.
Киселине и базе проучава Неорганска хемија, грана која проучава једињења која нису створена угљеником.
Концепти киселина и основа
Концепт Аррениус-а
Један од првих концепата киселина и база који је крајем 19. века развио Сванте Аррхениус, шведски хемичар.
Према Аррхениус-у, киселине су супстанце које у воденом раствору трпе јонизација, ослобађајући као катионе само Х +.
ХЦл (вод.) → Х.+ (вод.) + Цл- (овде)
У међувремену, базе су супстанце које пате јонска дисоцијација, ослобађајући ОХ- (хидроксил) јоне као једину врсту аниона.
НаОХ (вод.) → На+ (вод.) + ОХ- (овде)
Међутим, Аррхениусов концепт киселина и база био је ограничен на воду.
Такође прочитајте о: Аррениусова теорија и Реакција неутрализације.
Концепт Бронстед-Ловри
Концепт Бронстед-Ловри је шири од Аррениус-овог и представљен је 1923. године.
Према овој новој дефиницији, киселине су супстанце способне за донирање протона Х.
+ другим супстанцама. А базе су супстанце способне да прихвате протон Х.+ осталих супстанци.То је киселина је донор протона, а база протонски рецептор.
Карактерише а јака киселина као онај који у потпуности јонизује у води, односно ослобађа Х јоне+.
Међутим, супстанца може бити амфипротична, односно способна да се понаша као киселина или Бронстед база. Погледајте пример воде (Х.2О), амфипротска супстанца:
ХНО3(вод.) + Х.2О.(л) → НЕ3- (вод.) + Х.3О.+(ак) = Бронстедова база, прихватила је протон
НХ3(вод.) + Х.2О.(л) → НХ4+(вод.) + ОХ-(ак) = Бронстед Ацид, донирани протон
Надаље, супстанце се понашају као коњуговани парови. Све реакције између киселине и а база Бронстед-а укључују пренос протона и имају два коњугована киселинско-базна пара. Погледајте пример:
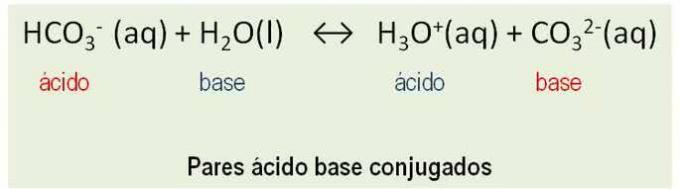
ХЦО3- и ЦО32-; Х.2О и Х.3О.+ су коњуговани парови киселинских база.
Сазнајте више о:
- Неорганске функције
- Индикатори киселинске базе
- Титрација
Номенклатура киселина
Да би се дефинисала номенклатура, киселине се деле у две групе:
- Хидрациди: киселине без кисеоника;
- Оксијакиселине: киселине са кисеоником.
Хидрациди
Номенклатура се јавља на следећи начин:
киселина + назив елемента + хид
Примери:
ХЦл = хлороводонична киселина
ХИ = хидриодна киселина
ХФ = флуороводонична киселина
оксиакиселине
Номенклатура оксиакиселина следи следећа правила:
ти стандардне киселине сваке породице (породице 14, 15, 16 и 17 Периодног система) следе опште правило:
киселина + назив елемента + иц
Примери:
ХЦлО3 = хлорна киселина
Х.2САМО4 = сумпорна киселина
Х.2ЦО3: угљена киселина
За остале киселине које се формирају са истим језгром, називамо их на основу количине кисеоника, следећи следеће правило:
| Количина кисеоника у односу на стандардну киселину | Номенклатура |
|---|---|
| + 1 кисеоник | Киселина + по + називу елемента + ицо |
| - 1 кисеоник | Киселина + назив елемента + кост |
| - 2 кисеоника | Киселина + хипо + назив елемента + кост |
Примери:
ХЦлО4 (4 атома кисеоника, један више од стандардне киселине): хлороводонична киселина;
ХЦлО2 (2 атома кисеоника, један мање од стандардне киселине): хлорна киселина;
ХЦлО (1 атом кисеоника, два мање од стандардне киселине): хлороводонична киселина.
Можда ће вас такође занимати: сумпорна киселина
Основна номенклатура
За основну номенклатуру поштује се опште правило:
Име хидроксида + катјона
Пример:
НаОХ = Натријум хидроксид
Међутим, када исти елемент формира катионе са различитим наелектрисањима, број наелектрисања јона додаје се на крај имена, римским бројевима.
Или можете додати суфикс -осо на најмање наелектрисани јон, а суфикс -ицо на наелектрисанији јон.
Пример:
Гвожђе
Вера2+ = Фе (ОХ)2 = Гвожђе ИИ хидроксид или железов хидроксид;
Вера3+ = Фе (ОХ)3 = Гвожђе ИИИ хидроксид или Жељезни хидроксид.
Обавезно проверите питања пријемног испита са предметом, са коментарисаном резолуцијом, у: Вежбе на неорганским функцијама.


