Редокс реакције укључују пренос електрона између атома, јона или молекула.
У реакцији оксидације-редукције долази до промена оксидационог броја (нок). Оксидација се састоји од процеса оксидације и редукције:
- Оксидација: Резултати губитак електрона и повећан нок.
- Смањење: Резултати добитак електрона и смањио нок.
Како се један елемент одриче електрона, други ће их примати. Дакле, укупан број примљених електрона једнак је укупном броју изгубљених електрона.
Примери редокс реакција на сагоревање, корозију и фотосинтезу.
Примери
У зависности од елемента који прима или донира електроне, имамо следећа имена:
- Редукционо средство: Онај ко се подвргне оксидацији узрокује смањење и повећава свој нок број. То је оно што губи електроне.
- Оксидирајуће средство: Онај који се подвргава редукцији, узрокује оксидацију и смањује његов нок број. То је оно што добија електроне.
О. оксидациони број представља електрични набој елемента у тренутку када учествује у а хемијска веза.
Ово стање је повезано са електронегативност, што је тенденција неких елемената да примају електроне.
1. Уочите први пример, имајте на уму да у реакцији између гвожђа и хлора долази до промене оксидационог броја. О. хлор јер је електронегативнији добија електроне:
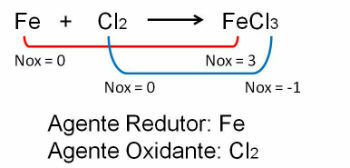
2. Реакција између гвожђа и кисеоника. Кисеоник је електронегативнији и на крају прима електроне и смањује њихов оксидациони број.
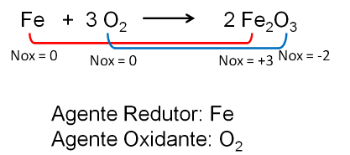
Сазнајте више, прочитајте такође:
- Оксидација
- Сагоревање
- Хемијске реакције
- електрони
Вежба решена
1. (ПУЦ-РС) У односу на једначину оксидације - неуравнотежена редукција Фе0 + ЦуСО4 → Фе2(САМО4)3 + Цу0, може се рећи да:
а) оксидациони број бакра у бакарном сулфату је +1.
б) атом гвожђа губи 2 електрона.
в) бакар се подвргава оксидацији.
г) гвожђе је оксидационо средство.
д) гвожђе пролази оксидацију.
Резолуција:
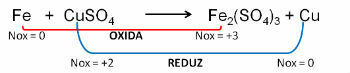
Одговорити:
д) гвожђе пролази оксидацију.
Вежбе
1. (УФАЦ-АЦ) У следећој хемијској једначини: Зн + 2 ХЦℓ → ЗнЦℓ2 + Х2
а) елемент Зн оксидира и реагује као оксидационо средство.
б) Зн елемент оксидира и реагује као редукционо средство.
в) Зн елемент се редукује и реагује као редукционо средство.
д) ХЦℓ је редукционо средство.
е) једначина је класификована као реверзибилна.
б) Зн елемент оксидира и реагује као редукционо средство.
2. (ИТА-СП) У јонској реакцији Ни (с) + Цу2+(ак) → Ни2+(вод.) + Цу (с)
а) никал је оксиданс јер је оксидисан.
б) никл је редуктор јер је оксидисан.
в) бакарни јон је оксидант јер је оксидисан.
г) бакарни јон је редуктор јер је редукован.
е) то није редокс реакција, стога нема оксиданса или редуктора.
б) никл је редуктор јер је оксидисан.
3. (УФРГС) Активно средство у белилу за домаћинство је хипохлорит-јон, ЦлО-. У процесима бељења овај јон се смањује; То значи да:
а) супстанца која подлеже дејству хипохлорита прима електроне.
б) долази до смањења броја електрона у његовој структури.
ц) ЦлО- је редукционо средство.
г) ЦлО- се претвара у елементарни хлор или хлоридни јон.
д) не врши се пренос електрона.
г) ЦлО- се претвара у елементарни хлор или хлоридни јон.


