Врење је промена из течног у гасовито стање. То се дешава када део течности, подвргнут датом притиску, прими топлоту и достигне одређену температуру.
Количина топлоте коју тело мора да прими да би се потпуно трансформисало у пару зависи од супстанце која га чини.
Супстанца у течном стању нема дефинисан облик, претпостављајући облик посуде која је садржи.
Будући да је практично неразумљив, представља кохезивну силу између честица које га чине.
Да би прешла у гасовито стање, супстанца мора примати топлоту. Ово повећање енергије учиниће да молекули вибрирају већим интензитетом, повећавајући растојање између њих.
На тај начин кохезиона сила практично не постоји. Тело у овом стању нема одређени облик или запремину.
Гејзири су примери кључања које се дешава са подземном водом која се налази у вулканским регионима. Магма загрева воду и када достигне одређену температуру почиње да мења стање.
Пара заузима већу запремину, повећавајући притисак у подземној шупљини. Као резултат, мешавина паре и течности избацује се на површину кроз мале пукотине.

Карактеристике кључања
Течност кључа по следећем обрасцу:
- Одржавајући константни притисак, температура током процеса кључања остаће константна.
- Количина топлоте по јединици масе потребна да би се течност потпуно претворила у пару назива се латентна топлота испаравања. Његова вредност зависи од супстанце која чини течност.
- Температура на којој свака супстанца кључа је добро одређена и назива се тачком кључања.
Савет: Када кувате храну, било би добро замерити ватру кад вода почне да кључа. Како температура остаје константна током читавог процеса кључања, време кувања биће исто и са великом или са малом. На тај начин штедимо гас и животна средина је захвална.
Количина латентне топлоте
Количина топлоте коју течност мора да прими да би се претворила у пару зависи од вредности латентне топлоте испаравања и њене масе.
У наставку представљамо вредност латентне топлоте испаравања неких супстанци:

Формула
Да бисмо израчунали количину топлоте потребне да би течност променила стање, користимо следећу формулу:
Где,
Кв: количина топлоте (креч)
м: маса (г)
Лв: латентна топлота испаравања (кал / г)
Пример:
Колико топлоте је потребно да 100 г етанола прокључа и потпуно се претвори у пару?
Кв = 100. 204 = 204 000 кал
Температура кључања
Температура на којој тело подлеже кључању зависи од супстанце која га сачињава и притиска којем је подвргнуто.
Тачка кључања супстанци одређује се у лабораторији. На пример, тачка кључања воде, подвргнуте 1 атмосфери, је 100 ° Ц. Гвожђе је 2800 ° Ц, док је водоник - 252,8 ° Ц.
Да бисте знали температуру промене фазе других супстанци, такође прочитајте тачка кључања.
Што је тело под мањим притиском, његова тачка кључања је нижа. То значи да је у градовима са великим надморским висинама потребно много више времена да се кува храна.
Да бисмо брже кухали храну, користимо шпорете под притиском. Ова врста шпорета користи систем заптивања који чини притисак у њој већим од атмосферског.
Већи притисак такође повећава тачку кључања. У случају воде, кључаће на температури која може достићи 120 ºЦ, смањујући време кувања.
фазне промене
Генерично се назива промена из течног у гасовито стање испаравање, јер обухвата, осим кључања, још два процеса: испаравање и грејање.
Испаравање се дешава постепено, без потребе да се достигне одређена температура. С друге стране, загревање се јавља када течност поставимо на површину која је на температури изнад тачке кључања.
Још увек постоје и други процеси промене стања. Да ли су они:
- Фузија
- Солидифицатион
- Укапљивање или кондензација
- Сублимација
На доњем дијаграму представљамо три физичка стања материје и одговарајуће промене стања:
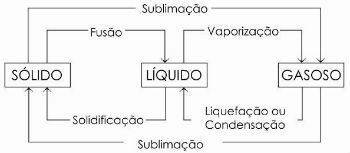
Да бисте сазнали више, прочитајте и ви Физичка стања воде.
Вежбе
Енем - 1999
Текст треба користити за следећа два питања.
Шпорети под притиском омогућавају кување хране у води много брже од уобичајених шпорета. Његов поклопац има гумену заптивку која не пушта пару да излази, осим кроз централну рупу на којој почива тег који контролише притисак. Када се користи, унутра се ствара висок притисак. За његов сигуран рад потребно је посматрати чистоћу централне рупе и постојање сигурносног вентила, који се нормално налази у поклопцу.
Шема шпорета под притиском и дијаграм водене фазе су представљени у наставку.
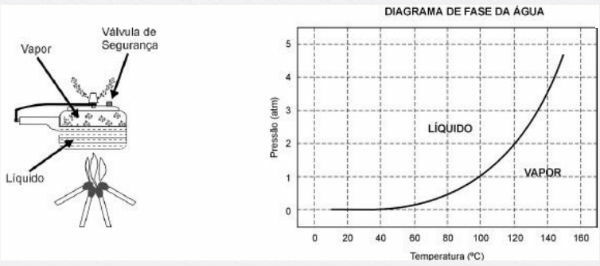
1) Предност употребе шпорета под притиском је брзина кувања хране и то због
а) притисак унутар њега, који је једнак притиску споља.
б) температура његове унутрашњости, која је изнад температуре кључања воде у месту.
в) количина додатне топлоте која се преноси у посуду.
д) количину паре коју испушта вентил.
е) дебљина зида која је већа од дебљине обичних шерпи.
Алтернатива б: на својој унутрашњој температури, која је изнад температуре кључања воде у месту.
2) Ако због економичности смањимо топлоту под шпоретом под притиском чим пара излази кроз вентил, како бисмо једноставно задржали време кључања, време кувања
а) биће већи јер се тава „охлади“.
б) биће мањи, јер смањује губитак воде.
в) биће већи како се притисак смањује.
г) биће већи како се испаравање смањује.
д) неће се мењати како се температура не мења.
Алтернатива е: неће се мењати јер температура не варира.


