О. атомски зрак елемената је периодично својство које одређује радијус атома који варира у зависности од положаја елемента у Периодном систему.
Тако се они могу повећавати и смањивати као атомски број (З) елемента који одговара броју протона присутних у језгру атома.
Укратко, атомски радијус одговара половини растојања између језгара два суседна атома, изражавајући се на следећи начин:
р = д / 2
одакле:
р = полупречник
д = интернуклеарна удаљеност
Генерално, атомски радијус се мери у пикометрима (пм), подмножним од метра (1 пикометар = 10-12 м.). Имајте на уму да када референца није атом већ јон, пронађени радијус је јонски радијус.
Варијација атомског радијуса
У периодном систему се раст атомског радијуса може видети на следећој слици:
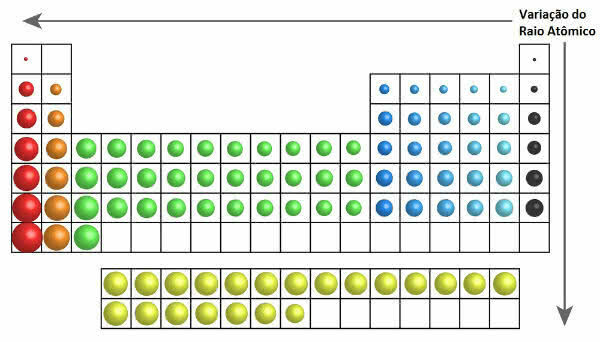 Варијација атомског радијуса у периодном систему
Варијација атомског радијуса у периодном систему
Тако се вертикално (породице или групе) атомски радијус повећава од врха до дна. На хоризонталном (тачке) повећавају се здесна налево.
Погледајте инверзну варијацију у Електронски афинитет и електронегативност.
Енергија јонизације
ТХЕ енергија јонизације (или потенцијал) такође је периодично својство које одређује енергију потребну за померање електрона, која се изражава у електрон-волтима (еВ).
Прочитајте такође: Периодична својства.
Проверите питања пријемног испита са коментарисаном резолуцијом у: Вежбе на периодном систему.

