Неутралишућа реакција се јавља када киселина реагује са базом да би створила воду и сол. Киселина даје Х јоне+ а база обезбеђује јоне ОХ- за стварање воде (Х.2О):
1 сат+(овде) + 1 ОХ-(овде) → Х.2О.(ℓ)
Ова врста реакције назива се „неутрализација“, јер се пХ средине неутралише; пХ воде је 7,0 (неутралан).
Да би се те реакције појавиле потребно је ослободити одређену количину топлоте, као само део енергије јони се користе за стварање веза које резултирају молекулима воде, док се остатак енергије ослобађа у прилично. Ова ослобођена енергија се назива Енталпија неутрализације (∆Хнеутрализација).

Пошто ослобађа топлоту, одговара егзотермним реакцијама, у којима ће енталпија (глобална енергија система) увек бити негативна, мања од нуле.
У случају реакције између јаких киселина и јаких база, вредност неутрализујуће енталпије увек ће бити једнака - 13,8 кцал / мол или - 57,7 кЈ / мол. То је зато што су базе и јаке киселине потпуно раздвојене у раствору и, према томе, једине Реакција одговорна за испољавање топлоте биће стварање воде, као што је приказано у три примера у наставку:
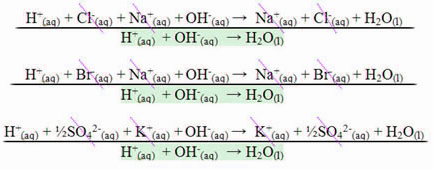
У случају реакција неутрализације које укључују слабе киселине или базе, вредност енталпије неутрализације биће мања од –57,7 кЈ / мол.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm
