Галијум је хемијски елемент са атомским бројем (З) једнаким 31 и његов симбол је Га. Припада породици 13 (или групи ИИИА, према старој нумерацији), која је породица бор, који је метал у боји „сребра“ сличан алуминијуму.
Једно од његових најзанимљивијих својстава је тачка топљења, која је ниска у поређењу са скоро свим металима (осим живе) који су раније познати, приближно 29,76 ° Ц. Дакле, под амбијенталним условима је обично у чврстом стању. Међутим, током топлијих дана топи се у течно стање. Зато, ако држимо овај метал у рукама, он ће почети да се топи, јер је наша температура виша од његове тачке топљења.

При складиштењу галијума не може напунити читав контејнер јер се шири док се стврдњава
На интернету постоји много видео записа који приказују кашику која се топи кад се стави у чашу воде. Заправо су ове кашике направљене од галијума, а не од других чешћих метала или металних легура попут алуминијума или челика. Дакле, када се калијска кашика стави у топлу воду, она постаје течност. О томе погледајте више у тексту „Предлог експерименталне класе на тачки топљења”.
Галијум има и још једну другачију особину, а то је огроман распон између температура топљења и кључања. Као што је већ поменуто, његова тачка топљења је око 29,76 ° Ц, али тачка кључања око 2204 ° Ц.
Галијум је открио француски хемичар Паул Лецок де Боисбаудран између 3:00 и 4:00 ујутру 27. августа 1875. године. Занимљив је аспект да је годинама раније, 1868. године, руски хемичар Димитри Иванович Мендељејев (1834-1907) предложио је Периодни систем, али је оставио празнину за елемент који је до тада био непознат. Менделејев га је назвао ека-алуминијум, јер је спектакуларно предвидео да ће у хоризонталном реду бора, између алуминијума и уранијума, лежати овај елемент.
Не заустављај се сада... После оглашавања има још;)

Француски хемичар Паул Лецок де Боисбаудран - откривач галијума
Мендељејев је чак предвидео својства овог елемента, попут његове атомске тежине, која би била 68, и његове специфичне тежине, која би била 5,9. Тако је Лецок открио елемент са атомском тежином од 69 и специфичном тежином од 4,7, што указује да је Менделејев погрешио. Међутим, Мендељејев је рекао да Лецоков узорак није довољно чист и да би требало да понови експерименте.
То је учинио Лецок, и изненађујуће је Менделеиев био у праву, специфична тежина овог новог елемента била је 5,9. Дакле, заиста је то био ека-алуминијум који је Мендељејев замислио.
Лецок је откривеном елементу дао име „Галијум“ у односу на латински назив за Француску, а то је Галија. Али постоје неки који кажу да им је у ствари био други циљ, јер на француском Ле цок значи „петао“, а на латинском галлус.
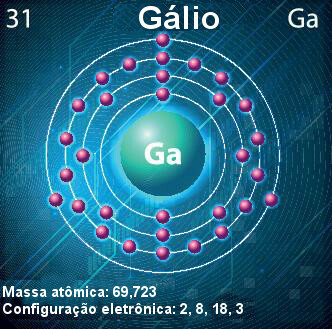
Атом галијума - симбол, атомски број, атомска маса и електронска конфигурација
Још једно својство галијума је да кородира друге метале. На Интернету постоје неки видео снимци који приказују постављање мало течног галијума на врх алуминијумске лименке. После неколико сати могуће је врло лако разбити рукама.
Међу применама галијума можемо истаћи:
* Користи се у производњи огледала;
* То је полупроводник и проводи топлоту двоструко више од гвожђе. Због тога се користи у производњи диода, ЛЕД-а, транзистора и сензора температуре, светлости и магнетног поља;
* У термометрима који се користе за врло високе температуре;
* У производњи легуре метала које треба да имају ниске тачке топљења;
* Добијање гаса водоника контактом између легуре алуминијумског галијума и воде;
* Изотоп Га-37 је радиоактиван и користи се као трагач у тестовима за откривање болести и тумора.
Јеннифер Фогаца
Дипломирао хемију
