ти Угљоводоници састављени су од угљеник (Ц) и водоник (Х). Флексибилност угљеника, који је главни елемент ових једињења, фаворизује постојање огромне разноликости структура Због тога се нека својства, попут тачке топљења и тачке кључања, могу разликовати између појединих угљоводоника.
То су углавном молекули аполар, са снагес интермолекуларни индуковани диполни тип и густина мања од Тхе од воде. Идентификација ових једињења може се извршити путем номенклатуре која следи правила успостављена од Међународне уније за чисту и примењену хемију (Иупац).
Прочитајте такође: Угљеник - један од најзаступљенијих елемената у Универзуму
Особине угљоводоника

Поларитет: угљоводоници без присуства хетероатома су аполар.
Међумолекуларне снаге: везе између молекула угљоводоника су тог типа индуковани дипол.
тачка топљења и икипећи: варирају у зависности од величине, функције и структурне организације молекула.
физичко стање: у нормалним условима температуре и притиска, угљоводоници са четири или мање атома угљеника су у гасовитом стању. Они са 5 до 17 угљеника су у течном стању, а угљоводоници са више од 17 угљеника су чврсте супстанце.
Густина: је мањи од густина воде, односно мање од 1,0 г / цм3.
Реактивност: алифатски и незасићени угљоводоници су слабо реактивни; незасићена једињења имају већу вероватноћу да реагују са другим молекулима, а циклични угљоводоници са до пет угљеника су врло реактивни.
Класификација угљоводоника
Угљоводоници могу се класификовати према структурној организацији ланца и по установама.Незасићење је присуство двоструке (их) или троструке везе између угљеника, је појава прикључци типа пи (π). већ је гране они су попут „грана“ везаних за већу структуру угљоводоника. Циклични ланци такође могу садржати гране и / или незасићења - структурна организација угљоводоника затвореног ланца формира полигоне као што су квадрат, троугао, хексан, између осталог.
У погледу распореда атома, угљоводоник може имати нормалан или разгранат ланац.
→ Ц угљоводоникнормална, линеарна или равна линија: онај са низом који има само два краја.

→ Ц угљоводоникмрзи разгранати: онај са ланцем који има више од два краја. Да бисте знали где су и које су гране, важно је правилно одабрати главни ланац. Главни ланац мора садржавати све незасићења и хетероатоме (ако постоје), добро као највећи број секвенцијалних угљеника. Угљеници који нису садржани у главном ланцу су гране.
Пример:

С обзиром на своје „затварање“, угљоводоник може имати затворени, отворени или мешани ланац.
→ Ланчани угљоводоницис затворено или циклично: они са ланцима у којима се атоми организују формирајући циклус, полигон или ароматични прстен (затворени угљоводоник са наизменичним незасићењима). Немојте имати лабаве крајеве ако нема гране. Сваки врх полигона представља угљеник и одговарајуће агенсе за везу водоника.
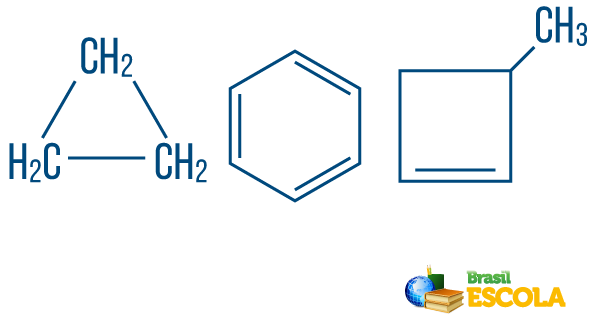
→ Отворени ланац или ациклични угљоводоници: су они са ланцима који имају најмање два краја.

→ Угљоводоник од низ мешовитог типа: је формиран прстеном или цикличним ланцем причвршћеним за линеарни део; има бар један крај.
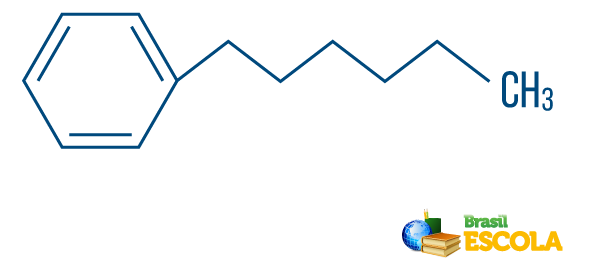
Прочитајте такође: Ароматични угљоводоници - примери и својства
Номенклатура угљоводоника
За сваку врсту угљоводоника постоји правило именовања које је успоставио Иупац. Номенклатура ових једињења је урађена на следећи начин:
1. део: локација и назив филијале (ако постоје);
2. део: термин се примењује циклус ако је једињење затворени ланац, али ако је алифатски (отворени) ланац, неће бити потребно;
3. део: префикс који показује колико угљеника има у главном ланцу;
4. део: локација и инфикс који указују на врсту незасићења у молекулу;
5. део: суфикс „о“ својствен угљоводоницима.
Ако молекул има отворену структуру, без гранања, номенклатура ће започети у 3. делу.
Следећа табела приказује потребне информације (префикс, инфикс и суфикс) за угљоводоничну номенклатуру уопште. О. префикс варира у зависности од броја угљеника; О. инфик, према броју незасићења; то је суфикс“О " Односи се на једињења типа угљоводоника.
Префикс |
Инфик |
Суфикс |
||
1 угљеник |
мет- |
Само појединачни позиви |
-ан- |
-О |
2 угљеника |
ет- |
|||
3 угљеника |
проп- |
1 двострука веза |
-ен- |
|
4 угљеника |
али- |
|||
5 угљеника |
пент- |
2 двоструке везе |
-диен- |
|
6 угљеника |
хек- |
|||
7 угљеника |
хепт- |
1 трострука веза |
-у- |
|
8 угљеника |
окт- |
|||
9 угљеника |
не- |
2 троструке везе |
-диин- |
|
10 угљеника |
дец- |
Први корак у откривању номенклатуре органског једињења је идентификовати главни ланац угљеника, који морају садржати незасићења и што више секвенцијалних угљеника. Након идентификовања главног ланца, угљеници морају бити набројани - започињање бројања са стране најближе гранама и незасићења (ако их има). ТХЕ локализација ће бити број угљеника на коме се налази грана или незасићење. Понекад постоји само једно могуће место радикалне или двоструке или троструке везе, тако да није потребно изразити место повезујућег угљеника у номенклатури.

ТХЕ номенклатура за огранке биће дато бројем угљеника у сваком, плус завршетак линија или лл. Када постоји више грана, користи се абецедни редослед.
Погледајте примере испод:
→ Пример 1
ЦХ3 - ЦХ2 - ЦХ3 → Пропан
1. део: префикс „проп-”Означава да ланац има три угљеника.
2. део: инфикс "-ан-”Сигнализира да молекул само успоставља везе типа сигма или једноставно.
3. део: суфикс "-О”Карактеристично је за угљоводонике.
→ Пример 2
ЦХ2= ЦХ-ЦХ2-ЦХ3 → Али-1-ен
У угљоводоницима са незасићеном површином потребно је нумерисати и лоцирати угљеник у којем се пар налази, а нумерисање мора бити што мање. У ту сврху, број угљеника мора почети са страницом која је најближа двострукој вези.
1. део: "али-" указује на то да у ланцу постоје четири угљеника.
2. део: "1-ен" односи се на незасићење смештено између угљеника 1 и 2.
3. део: "-О" је карактеристични суфикс угљоводоника.
→ Пример 3

1. део: "3-етил" сигнализира да на угљенику 2 постоји грана од два угљеника.
2. део: "-пент-" указује на присуство пет угљеника у главном ланцу.
3. део: "-ан-" је инфикс који се примењује на незасићене ланце (без двоструких или троструких веза).
4. део: "-О" је карактеристични суфикс угљоводоника.
→ Пример 4
За ланце са више грана, сместите радикале у номенклатуру по абецедном реду. Ако у истом молекулу постоје гране и незасићења, бројање угљеника у главном ланцу треба извршити тако да збир бројева локација буде што мањи.
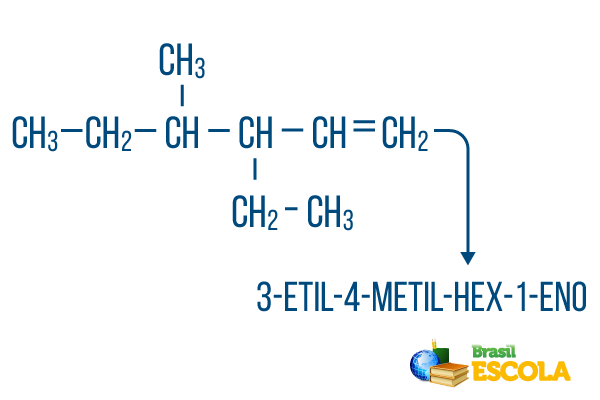
Бројање угљеника у главном ланцу извршено је слева надесно, а збир бројева незасићења и места грана је: 1 + 4 + 3 = 8. Да је број угљеника био здесна налево, сложена номенклатура би била 4-етил-3-метил-5-ен, чији би збир локација био: 4 + 3 + 5 = 12, што је веће од друге хипотезе, па је не би требало користити.
1. део: 3-етил-4-метил упућује на радикале по абецедном реду и на њихова места.
2. део: хек- значи да у главном ланцу има 6 угљеника.
3. део: 1-ен указује на присуство двоструке везе на угљенику 1.
4. део: "-О" је карактеристични суфикс угљоводоника.
→ Пример 5
За затворене низове важе правила за именовање, али реч циклус започиње назив једињења, указујући да је то затворени или циклични угљоводоник.
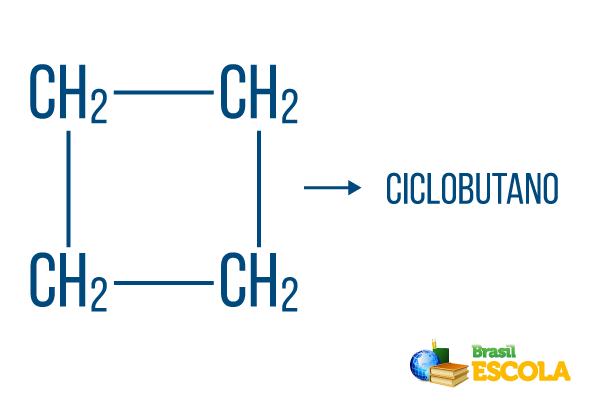
1. део: циклус- означава да је то затворени низ.
2. део: -али- означава постојање 4 угљеника у ланцу
3. део: -Оје карактеристични суфикс угљоводоника.
Прочитајте такође: Класификација ланаца угљеника
Врсте угљоводоника
Угљоводоници се могу поделити на алкане, алкене, алкине и алкадиене - који се класификују као према успостављању ланца (двоструке (е) или троструке везе) - и циклана, који су ланци затворено.
→ Алкани: су угљоводоници који немају незасићење. Општа формула за алкане је Ц.неХ.2н + 2, и непредзнак саставља га префикс + ан + О.
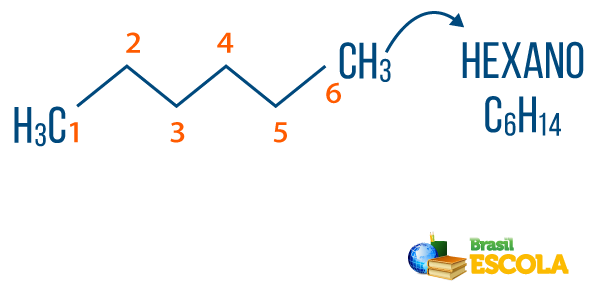
ти алкани могу се наћи у природи, попут бензина метан (ЦХ4), коју животиње ослобађају и производе у процесима разградње, као и у рафинеријама и петрохемијској индустрији. Једињења попут пропан (Ц3Х.7), бутан (Ц4Х.10), који чини наш гас за кување (ТНГ), и октан (Ц8Х.18), присутни у аутомобилском гориву, су нуспроизводи од Нафта.

→ алкени или алкени: су ланци угљеника који имају незасићење, двоструку везу. Његова општа формула је Ц.неХ.2н, и твоје непредзнак саставља га П.поправити + ен + о.

О. етилен гас (Ц2Х.4), који се у пољопривреди користи за убрзање сазревања плодова, припада функцији алкен. Једињење се такође користи у производњи сировина полиетилен, користи се у производњи пластичног посуђа.
→ Алкини или ацетиленски: угљоводоници са троструком везом. Његова општа формула је Ц.неХ.2н - 2. ТХЕ номенклатура саставља га префикс + у + о.

О. ацетилен или етин (Ц.2Х.2) је гас алкинске функције који се користи у шавова и металних резова. Ово једињење може да достигне температуре и до 3.000 ° Ц, што омогућава поправке на потопљеним деловима брода.

→ алкадиене или диене: ланци угљеника са две незасићења, односно две двоструке везе између угљеника. Општа формула за ову функцију је Ц.неХ.2н - 2. Схватите да је то иста формула као и алкини, што значи да се то може догодити изомеризам између једињења (иста молекулска формула за различита једињења).
Номенклатура алкадиене састоји се од П.поправити + диен + о.
Пример:

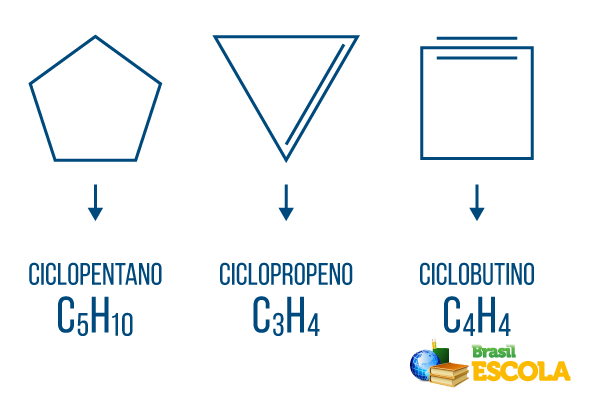
→ Угљоводоници затвореног ланца: молекули се организују на цикличан начин, имају тенденцију да образују полигон и, баш као што се у отвореним ланцима могу појавити установе и / или последице. Циклони, циклони, циклини и бензени су угљоводоници затвореног ланца.
Циклони или циклоалкани: циклични ланци који се састоје само од једноструких веза. Његова општа формула је Ц.неХ.2н. Номенклатура: вицло + префикс + ан + о.
Циклуси или циклоалкени: затворени ланци угљоводоника са објектом. Његова општа формула је Ц.неХ.2н-2. Номенклатура: цицло + префикс + ен + О..
-
Циклини или циклоалкини: угљоводоници затвореног ланца са присуством две двоструке везе. Његова општа формула је Ц.неХ.2н-4. Номенклатура: цицло + префикс + у + о.
бензени
Бензен је врста угљоводоника затвореног ланца са шест угљеника где се везе разликују између једноструких и двоструких. Ова једињења су отровно и високо канцероген, користи се као органски растварач у хемијским процесима.
Да би се угљоводоник сматрао ароматичним, мора да постоји најмање један бензенски прстен, који је високо реактиван, па подлеже двема или више замене, што ћемо овде видети као последице. Када постоје два радикала која повезују, имат ћемо одређена имена за сваки пар положаја.
Радијали на 1,2 угљеника бензена → орто
Радикали на 1,3 угљеника бензена → циљ
Радијали на угљенику 1,4 бензена → за
Анноменклатура ароматичног једињења врши се на следећи начин:
1. део: позиционирање лиганда (орто, циљ или да).
2. део: назив радикала или радикала везаних за бензен (метил, етил, пропил ...). Име радикала даје правило осталих угљоводоника.
- 3. део: -Б.отров, што је карактеристичан појам ароматичних угљоводоника.
Примери:
→ Орто-диметил-бензен

1. део: О.рто- указује да су радикали позиционирани на угљеницима 1 и 2.
2. део: -диметил- Односи се на два радикала, оба са једним угљеником.
3. део: -бензен је карактеристичан термин за ароматичне угљоводонике.
→ Орто-етил-метил-бензен
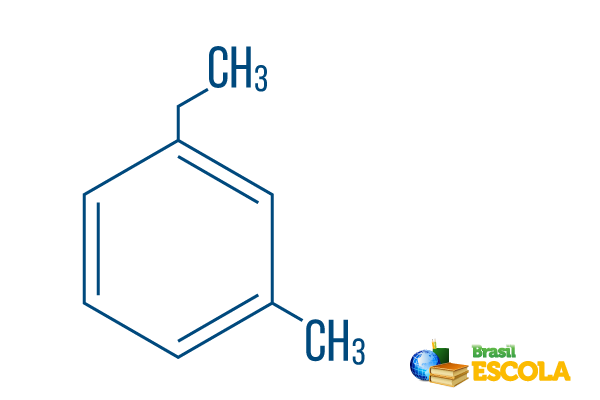
1. део: мох- показује да су радикали позиционирани на угљеницима 1 и 3.
2. део: етил-метил- Односи се на количину угљеника у сваком радикалу, тј етил Тхе двокарбонска грана и метил гранање са једним угљеником - стављено у номенклатуру по абецедном реду.
3. део: -бензен је карактеристичан термин за ароматичне угљоводонике.
→ Пара-диетил-бензен
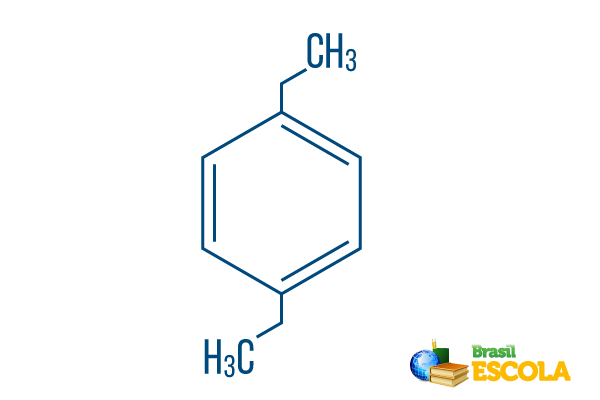
1. део: П.плуг указује да су радикали на угљеницима 1 и 4 бензена.
2. део: -диетил- упућује на два радикала тог типа етил, односно две гране са по два угљеника.
3. део: -бензен је карактеристичан термин за ароматичне угљоводонике.
Прочитајте такође:Откриће структуре бензена
решене вежбе
(Унесп) - Октан је један од главних састојака бензина, који је мешавина угљоводоника. Молекулска формула октана је:
а) Ц8Х18
б) Ц8Х16
ц) Ц8Х14
д) Ц12Х24
е) Ц18Х38
Одговор: слово а). Анализирајући сложену номенклатуру октан, то је алкан, односно молекул који се састоји само од једноструких веза. Ако је општа формула за алкане Ц.неХ.2н + 2, заменом „н“ за осам, што је количина угљеника у главном ланцу - и јединствено у овом случају -, имаћемо да је молекуларна формула октана Ц8Х18.
(УФСЦар-СП) - Размотрите следеће изјаве о угљоводоницима.
И) Угљоводоници су органска једињења која се састоје само од угљеника и водоника.
ИИ) Само незасићени угљоводоници равног ланца називају се алкени.
ИИИ) Циклоалкани су засићени алифатски угљоводоници опште формуле ЦнХ2н.
ИВ) Да ли су ароматични угљоводоници: бромобензен, п-нитротолуен и нафтален.
Следеће изјаве су тачне:
а) само И и ИИИ.
б) само И, ИИИ и ИВ.
в) само ИИ и ИИИ.
г) само ИИИ и ИВ.
е) само И, ИИ и ИВ.
Одговор: Слово а).
ИИ - Алкени су једињења са двоструком везом, односно незасићена, али у свом ланцу могу имати последице, а не искључиво линеарно.
ИВ - Брометобензен и п-нитротолуенска једињења припадају другим органске функције.
аутор Лаиса Бернардес
Наставник хемије
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/hidrocarbonetos.htm
