Дисоцијација базе то је физички процес који се јавља код ове важне групе неорганских супстанци када се растворе у води, или када прођу кроз процес фузије (прелазак из чврстог у течно стање кроз грејање).
Генерално, феномен дисоцијација базе то је ослобађање катиона и ањона који формирају јонско једињење, која је, у овом случају, основа. Дакле, током дисоцијација базе, пуштање јони који већ постоје у једињењу, односно не формирају се нови јони.
Базу формира било који метал (Кс), који је катион једињења, или амонијум-катион (НХ група)4+), везан за хидроксид анион (представљен ОХ групом), као у приказима испод:
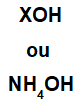
Општи прикази основне формуле
облик представљају дисоцијација базе то се врши кроз једначину у којој у реактанту имамо базу, а у производима јоне (катионе и анионе). Оно што чини разлику је како се одвија дисоцијација:
Растварање базе у води:
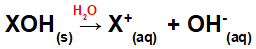
Једначина која представља дисоцијацију базе у воденом медијуму
Дисоцијација основним спајањем:
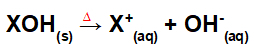
Једначина која представља дисоцијацију базе поступком фузије
Анализирајући горње опште једначине, потврђујемо да ћемо у свима њима увек имати базу, катион (а то је метал или НХ група4+) и анион (ОХ-). Али да ли су сви такви? Нема ли разлике међу њима? На прво питање одговор је не, а на друго питање је да.
Не заустављај се сада... После оглашавања има још;)
Када извршимо дисоцијација од базе, основно је прво анализирати основну формулу, јер из ње можемо одредити оптерећење катион и мол количина хидроксидних ањона, пошто је мол количина катиона стандардна (увек 1 мол).
Вреди подсетити да количина ОХ група присутних у основној формули одређује наелектрисање катјона и количину у молу хидроксидног аниона у дисоцијацији базе.
Погледајмо примере алуминијум хидроксида [Ал (ОХ)3] и златни хидроксид (АуОХ). У основној формули алуминијума постоје три ОХ групе, а у златној формули само једна ОХ група. Дакле, у дисоцијацији ових основа имамо:
Ал (ОХ) дисоцијација3:
Како ова база има три ОХ групе у формули, наелектрисање на катиону биће +3, а количина у мол аниона једнака је 3 мола, као што можемо видети у следећој једначини:
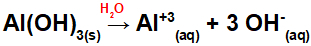
Једначина дисоцијације базе алуминијума у воденом медијуму
Дисоцијација од АуОХ:
Како ова база има ОХ групу у формули, наелектрисање на катиону биће +1, а количина у мол аниона једнака 1 мол, као што можемо видети у следећој једначини:
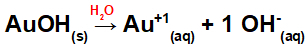
Једначина дисоцијације базе са златом у воденом медијуму
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или академском раду? Погледајте:
ДАНИ, Диого Лопес. „Шта је дисоцијација базе?“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm. Приступљено 27. јуна 2021.
Хемија

Дисоцијација и јонизација, италијански научник Волта, електрична струја, шведски физички хемичар Свант Аугуст Аррхениус, теорија Аррениус, позитивни јони, катиони, негативни јони, аниони, каустична сода, кухињска со, поларни молекули, дисоцијација јонски,