О. израчунавање броја атомских честица користи се за означавање количине протона (у језгру), електрона (у електросфери) и неутрона (у језгру) присутних у било ком атому или јону. Да бисте то урадили, неопходно је знати неке карактеристике атома:
1- Атомски број (З)
То је математички код, представљен великим словом З, позициониран на доњој левој страни скраћенице атома:
З.Икс
Означава број протона (п) у језгру и број електрона (е) у електросфери атома. Дакле, уопштено речено:
З = п = е
2- Масни број (А)
То је математички код који одговара збиру броја протона (п) и неутрона (н), оба присутна у језгру било ког атома. Једначина која представља масени број дата је:
А = п + н
Будући да је број протона једнак атомском броју, можемо написати једначину за израчунавање масеног броја на следећи начин:
А = З + н
Ако знамо масени број и атомски број атома, можемо утврдити број неутрона на следећи начин:
н = А - З
3- јони
Они су атоми који губе или добијају електроне. Они имају позитиван или негативан знак позициониран у горњем десном углу њиховог приказа, као у следећем моделу:
Икс+ или Кс-
Позитивни јон: То се назива катионом, а позитивни знак указује на то да је изгубио електроне.
Негативни јон: То се назива анионом, а негативни знак указује да је стекао електроне.
Не заустављај се сада... После оглашавања има још;)
4- Атомске сличности
а) Изотопи
Атоми који имају исти атомски број и различите масене бројеве. Пример:
7Икс14 и 7И16
Атоми Кс и И имају исти атомски број (лево од скраћенице), односно једнак 7. Атом Кс има масени број (с десне стране скраћенице) једнак 14, а атом И има масени број једнак 16.
б) изобаре
Атоми који имају исти масени број и различите атомске бројеве. Пример:
15Икс31 и 13И31
Атоми Кс и И имају масени број (десно од скраћенице) једнак 31. Атом Кс, с друге стране, има атомски број једнак 15, а атом И атомски број једнак 13.
в) Изотони
Атоми који имају различите масене бројеве и атомске бројеве, али исти број неутрона.
г) Изоелектроника
Атоми који имају исти број електрона. Пример:
12Икс+2 и 7И-3
Атом Кс има атомски број једнак 12 и катион је (са позитивним наелектрисањем +2), па губи два електрона, имајући тако 10 електрона у својој електросфери. Атом И, с друге стране, има атомски број једнак 7 и анион је (са негативним наелектрисањем -3), па добија три електрона, имајући тако 10 електрона у својој електросфери.
Мапа ума: Атомске честице
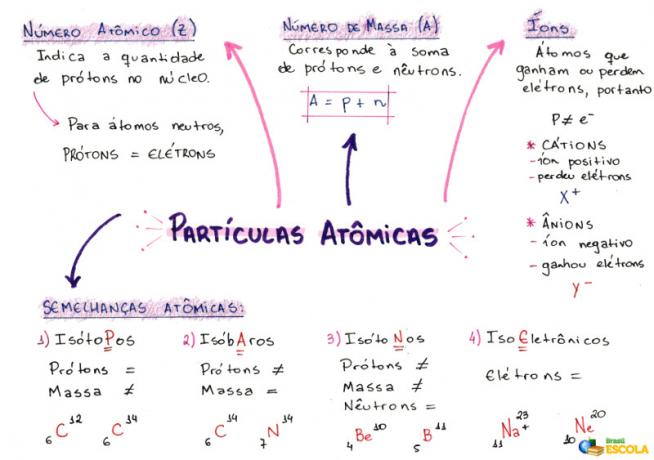
* Да бисте преузели мапу ума у ПДФ-у, Кликните овде!
Примери израчунавања броја атомских честица
Пример 1: Одредити број протона, неутрона и електрона у атому 14Икс29.
Дате су следеће вредности за атом Кс:
Број масе (горе десно) = 29
Атомски број (доле лево) = 14
Да бисте одредили број протона:
Број протона је увек једнак атомском броју, па Кс атом има 14 протона.
Да бисте одредили број електрона:
Како атом Кс није јон, стога је број електрона једнак броју протона, односно 14.
Да бисте утврдили број неутрона:
Број неутрона одређује се помоћу броја масе и протона у следећој формули:
А = п + н
29 = 14 + н
29 - 14 = н
н = 15
Пример 2: Одредити број протона, неутрона и електрона јона Кс+3, знајући да су њихов масени број и атомски број 51, односно 23.
Дате су следеће вредности за јон Кс:
Масени број = 51
Атомски број (доле лево) = 23
Да бисте одредили број протона:
Број протона је увек једнак атомском броју, па Кс атом има 23 протона.
Да бисте одредили број електрона:
Јон Кс је позитиван (+3), па је то катион који је изгубио три електрона. Дакле, његов број електрона је 20.
БЕЛЕШКА: Смањење или повећање броја електрона се увек јавља у односу на атомски број.
Да бисте утврдили број неутрона:
Број неутрона одређује се помоћу броја масе и протона у следећој формули:
А = п + н
51 = 23 + н
51 - 23 = н
н = 28
Пример 3: Атом В има атомски број и масу једнаку, односно 29 и 57, што је изобаре од а атом И, који има атомски број једнак 30, што је изотоп атома Б, чији је масени број 65. Помоћу ових података одредите број протона, неутрона и електрона у атому Б.
Подаци добијени вежбом:
Атом В.
атомски број (доле лево) = 29
масени број (горе десно) = 57
И изобар, односно маса И је такође 57.
И атом
атомски број = 30
масени број = 57
Са ове две вредности морамо одредити његов неутронски број јер је то изотон елемента Б:
А = З + н
57 = 30 + н
57 - 30 = н
н = 27
Атом Б:
масени број = 65
број неутрона = 27
Са овим подацима морамо одредити његов атомски број, јер ћемо помоћу тога одредити његов број протона и број електрона (јер то није јон):
А = З + н
65 = З + 27
65 - 27 = З
З = 38
Према томе, атом Б има 38 протона, 38 електрона и 27 неутрона.
* Минд Мап, Вицтор Рицардо Ферреира
Наставник хемије
Ја сам, Диого Лопес Диас