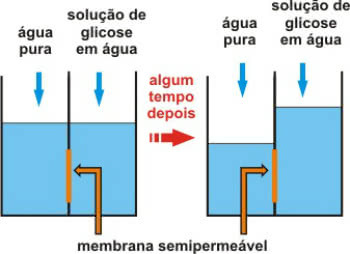
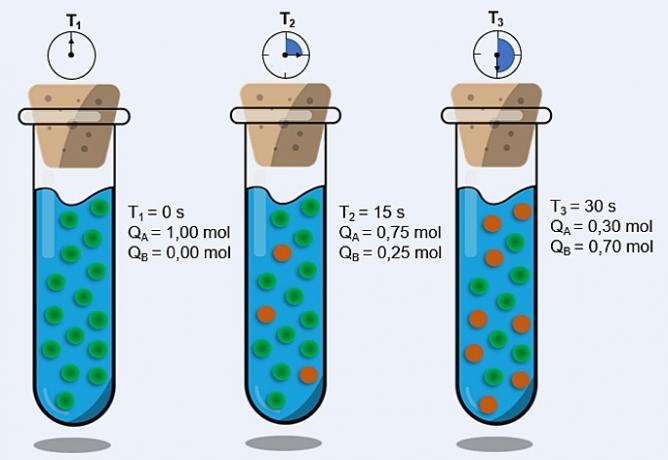
Гас који садржи сода коју конзумирамо је угљен-диоксид (угљен-диоксид - ЦО2). Расхладно средство се генерално формира из воденог раствора неке врсте сирупа и овог гаса. Али пре него што мешају гас у сирупу, произвођачи мешају воду и гас у уређају који се назива карбонизер, генеришући угљену киселину која има течни облик. У овој врсти пића тада постоји следећа хемијска равнотежа:
2 сата2О.(1) + 1 ЦО2 (г) ↔ 1 сат3О.+(овде) + 1 ХЦО1-(овде)
Ле Цхателиер-ов принцип каже да када се неки облик поремећаја изазове у хемијском систему, његова равнотежа се помера ка смањењу тих поремећаја.
Када пијемо соду, неколико система се мења, мењајући хемијску равнотежу на различите начине.
На пример, у нашем желуцу постоји желучани сок који се углавном формира од хлороводоничне киселине (ХЦл). Ова киселина, као и све друге, карактерише присуство јона Х+ или Х.3О.+ у воденом медијуму. Због тога присуство киселине у желуцу повећава концентрацију Х.3О.+ у описаној равнотежи и, према томе, помера равнотежу расхладног средства у обрнутом смеру реакције, на леву страну хемијске једначине. То значи да ће доћи до више стварања угљен-диоксида.


Ово је један од фактора који узрокује такозвано подригивање (подригивање) након пијења газираних пића.
Остали фактори који такође узрокују ово су смањење притиска и повећање температуре. Када се расхладно средство производи, угљен-диоксид се раствори у течности под два услова: врло високим притиском и ниским температурама. У тим условима гас постаје течност и пуни се у боце. Због тога сода фабрике оставља хладним.
Не заустављај се сада... После оглашавања има још;)
Али када дође до нашег желуца, температура је много виша, а притисак нижи. Погледајте како ово утиче на равнотежу:
- Смањење притиска:
Када се притисак гасовитог система смањи, то узрокује ширење запремине гаса и равнотежа се помера на страну веће запремине (већи број молова). Имајте на уму да је у равнотежи коју разматрамо запремина гаса већа на левој страни (реактаната), јер она једина садржи 1 мол угљен-диоксида.
Дакле, смањење притиска помера ову равнотежу у смер обрнуте реакције, повећавајући количину ЦО2 у систему.
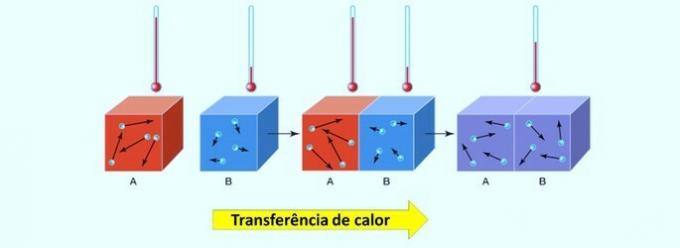
- Повећање температуре:
Пошто је растворљивост ЦО2 у води се смањује како температура расте, када достигне наш стомак, чија је температура око 36 ºЦ, овај гас се ослобађа. Дакле, као и у претходним случајевима, фаворизована је и обрнута реакција. Осећај свежине који осећамо када пијемо безалкохолно пиће резултат је ширења угљен-диоксида, који је ендотермни процес, односно он упија топлоту из нашег тела.
Смањење притиска и пораст температуре не дешавају се само у нашем стомаку. То можемо видети чим отворимо боцу с содом и гас се ослободи док спуштамо притисак. Такође, можда сте приметили да што је расхладно средство вруће, више гаса ће из њега изаћи.

Јеннифер Фогаца
Дипломирао хемију
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ФОГАЊА, Јеннифер Роцха Варгас. „Хемијска равнотежа соде у стомаку“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/equilibrio-quimico-refrigerante-no-estomago.htm. Приступљено 28. јуна 2021.
Хемија

Проверите своје знање и научите више помоћу ове листе решених вежби на хемијским вагама. Кроз овај материјал моћи ћете боље да разумете како се раде константе равнотеже (Кп, Кц и Ки), померање равнотеже, пХ и пОХ, као и равнотежа у такозваним пуферским растворима.