Етер то је кисеонична органска функција, односно има хемијски елемент кисеоник, поред угљеника и водоника. Ова функција има за главну структурну карактеристику присуство двоје органски радикали везан за атом кисеоника.
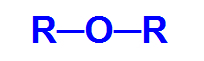
Општа структурна формула етра
Дакле, ланац угљеника у етру је хетероген и може имати два идентична или различита радикала алкил, врсте радикала који немају ароматичну структуру, или арил, радикали који немају структуру ароматичан.
Физичке карактеристике етра
Што се тиче физичког стања на собној температури: када етер у свом саставу има четири или више атома угљеника, течан је;
Што се тиче тачке топљења и тачке кључања: у поређењу са другим масним органским једињењима приближни молари, имају тачку топљења сличну тачки алкана и нижу од осталих једињења органска;
Што се тиче густине: то су једињења која имају малу густину у поређењу са водом;
Што се тиче сила интеракције: етери су састављени са малим поларитетом, међусобно комуницирају кроз слабу трајну диполну интеракцију. Са водом и алкохолима, етери имају способност интеракције водоничним везама.
Што се тиче поларитет: су једињења која имају угаону геометрију, дакле, поларна су.
Што се тиче органолептичких карактеристика: то су супстанце које дају врло пријатан мирис, али њихово удисање може изазвати зависност.
Службена номенклатура етра
Префикс мањег стабла + окси + префикс главног стабла + инфикс + о
Да би се извршила званична номенклатура а етер, Кључно је одредити који је ваш главни лиганд, а који мањи. Да бисте то урадили, следите два примера примене овог правила именовања у наставку:
1. пример:
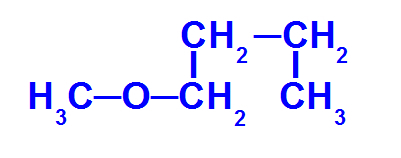
Структурна формула етра са мање угљеника
Горњи етар има следеће радикале:
Метил (ЦХ3-);
Бутил (ЦХ3-ЦХ2-ЦХ2-ЦХ2-).
Да бисмо именовали ово једињење, имамо:
мањи радикални префикс: Мет
+
окси
+
главни матични префикс: али
+
ан (јер има само појединачне везе)
+
О.
Дакле, име овога етер то ће бити метоксибутан.
2. пример:
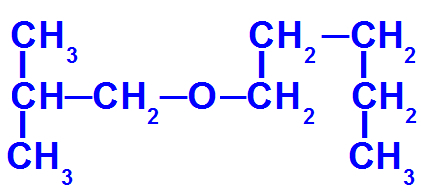
Структурна формула етра са више угљеника
Овај етар има следеће радикале:
Изобутил [(ЦХ3)2-ЦХ-ЦХ2-);
пентил (ЦХ3-ЦХ2-ЦХ2-ЦХ2-ЦХ2).
Да бисмо то именовали, имамо:
мањи радикални префикс: исобут
+
окси
+
главни матични префикс: пент
+
ан (јер има само појединачне везе)
+
О.
Дакле, назив етер у питању ће бити изобутоксипентан.
Уобичајена номенклатура етра
Етер + назив радикала (најједноставнији, а затим и најсложенији) + ицо
или
Радикална имена + етар
Следите два примера примене овог правила именовања:
1. пример:

Структурна формула етра који има четири угљеника
То етер представља следеће радикале:
Метил (ЦХ3);
Изопропил (ЦХ3-ЦХ-ЦХ3).
Дакле, за ово једињење имамо:
Етер
+
споредни радикал: метил
+
главни радикални префикс: изопропил
+
ицх
Дакле, назив етер у питању ће бити метил изопропил етар, или метил изопропил етар.
2. пример:

Структурна формула етра који има пет угљеника
Горњи етар има следеће радикале:
Етил (ЦХ3-ЦХ2-);
Пропил (ЦХ3-ЦХ2-ЦХ2-).
Да бисмо именовали ово једињење, имамо:
Етер
+
споредни радикал: етил
+
главни радикални префикс: пропил
+
ицх
Дакле, назив етер у питању ће бити етил пропил етар, који такође може бити етил пропил етар.
Употреба етара
Генерално, етери се користе:
Као инертни органски растварачи, који не учествују ни у једној реакцији;
Користи се за вађење есенција, попут цвећа, дрвета итд .;
Користи се за екстракцију различитих уља и масти.
Ја сам, Диого Лопес
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eter.htm
