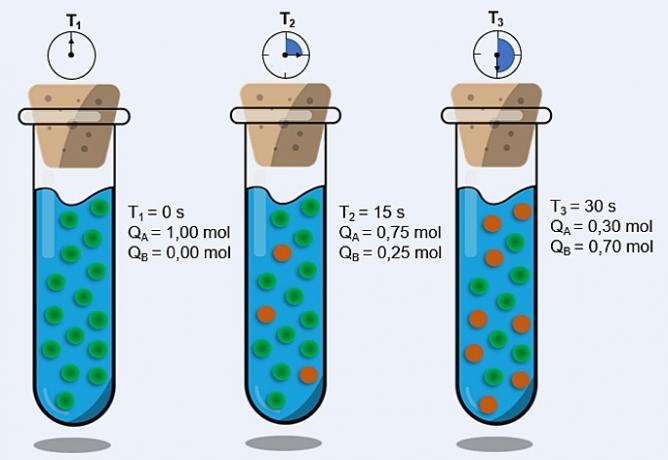
Za kemično reakcijo je treba izpolniti štiri osnovne pogoje, ki so:
1. Reagenti morajo stopiti v stik;
2. Med reagenti mora biti kemična afiniteta;
3. Trki med delci reagenta morajo biti učinkoviti;
4. Doseči je treba aktivacijsko energijo.
Na kratko si oglejte vsak primer:
1.Stik med reagenti:
Ta pogoj je očiten, saj tudi če imajo reaktanti veliko afiniteto drug do drugega, tako kot pri kislinah in bazah, če se ločijo, reakcija ne bo prišlo. Morajo priti v stik, da lahko njihovi delci trčijo, pretrgajo vezi reaktantov in tvorijo vezi izdelkov.

2.Kemična afiniteta:
Kot smo videli, je treba reagente navezati, vendar premalo. Če na primer natrij damo v stik z vodo, se bo zgodila izjemno silovita reakcija, če pa damo zlato, ne bomo videli nobene razlike. To je zato, ker imajo različne snovi različne kemijske afinitete med seboj ali pa sploh nimajo afinitete. Večja je kemijska afiniteta, hitrejša je reakcija.
V omenjenih primerih ima natrij veliko afiniteto z vodo, tako da se kovinski natrij shrani v kerozinu, da ne pride v stik z vlago v zraku. Zlato je inertno, zato zlati spomeniki trajajo tako dolgo, kot egiptovski sarkofagi.

3.Teorija trkov:
Tudi za spojine, ki imajo kemično afiniteto, je za reakcijo nujno, da njihovi delci, atomi ali molekule učinkovito trčijo. Vsi delci, ki trčijo, tega ne naredijo učinkovito, toda udarci, ki povzročijo zlom reagenske vezi in tvorbe novih vezi so tiste, ki se pojavijo v pravilni usmeritvi in z energijo dovolj.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Spodaj je prikazan primer dveh neučinkovitih trkov in enega učinkovitega trka, ki povzroči reakcijo.
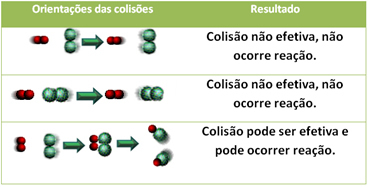
4.Aktivacijska energija in aktivirani kompleks:
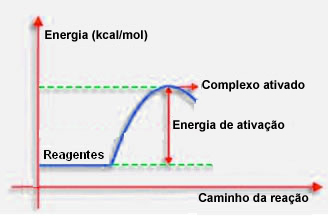
Kot je navedeno v prejšnji točki, učinkovito trčenje poleg ugodnih smernic potrebuje tudi dovolj energije. Najmanjša količina energije, ki je potrebna za vsako reakcijo, se imenuje aktivacijska energija.
Če imajo reaktanti med dobro usmerjenim udarcem energijo, ki je enaka ali večja od aktivacijske energije, tvori se prvotno aktiviran kompleks, ki je vmesna struktura med reaktanti in izdelkov. V aktiviranem kompleksu nastajajo oslabljene reagenske vezi in nastajajo nove produktne vezi.
Tako aktivacijska energija deluje kot nekakšna ovira za nastanek reakcije, kajti večja kot je, težje bo prišlo do reakcije. V nekaterih primerih je treba reagente oskrbeti z energijo. Kuharski plin ima na primer afiniteto za interakcijo s kisikom v zraku, vendar moramo energijo oskrbeti, ko združimo vžigalico, sicer reakcija ne poteka. Toda ko se reakcija sproži, sprosti dovolj energije, da aktivira druge molekule in ohrani reakcijo.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Pogoji za pojav kemičnih reakcij"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm. Dostop 27. junija 2021.