Preden razumemo, kaj sploh gre za magnetno kvantno število in kvantno število vrtenje, treba si je zapomniti, kaj pomeni beseda orbital.
Orbital je območje vesolja okoli jedra, kjer je verjetnost iskanja določenega elektrona največja.
Za boljše razumevanje si omislite panj. Ni mogoče z gotovostjo reči o poti in položaju vsake čebele, lahko pa označimo regijo okoli panja, kjer najverjetneje najdemo čebele. Podobno orbita označuje območje okoli jedra atoma, kjer bo najverjetneje določen položaj elektronov.
Ker ima elektron dvojno značilnost, se pravi, da se obnaša kot delček in tudi kot val; znanstveniki ga raje prepoznajo glede na njegovo energijsko vsebnost. Z matematičnimi izračuni je znanstvenik Erwin Schrödinger leta 1927 povezal telesno naravo, energijo, naboj in maso elektrona. Tako so za vsak elektron značilna kvantna števila.
Kvantna števila so matematične kode, povezane z elektronsko energijo.
Dve najbolj znani kvantni številki sta glavno kvantno število (n) in sekundarno ali azimutno (
tam).Glavna označuje plast ali nivo energije (K, L, M, N, O, P, Q), v katerem se nahaja elektron, in sicer od 1 do 7. Azimut predstavlja energetske podnivoje (s, p, d, f), ki znašajo 0,1,2,3. Oboje se pojavlja v spodnjem energetskem diagramu, kjer glavno kvantno število predstavlja sedem "stopnic", sekundarno kvantno število pa "stopnice" stopnic.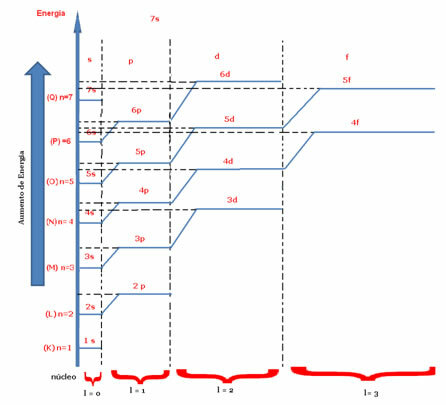
Zdaj pa razmislimo o magnetnem kvantnem številu in vrtenje:
- Magnetna kvantna številka (m ali mtam) → označuje orientacijo orbital v vesolju.
V skladu s spodnjim energijskim diagramom so vrednosti m predstavljene z majhnimi kvadratki (ali s kroglicami, odvisno od avtorja). Za vsako orbitalo imamo vrednost za magnetno kvantno število, ki se razlikuje od -tam The+1.

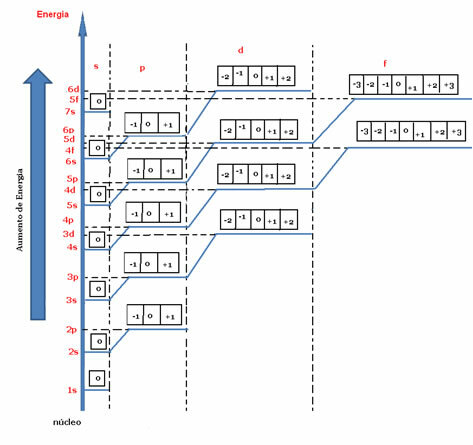
Energijski diagram, ki označuje magnetno kvantno število
-
Kvantna številka vrtenje (s ali ms)→Orbitala ima največ dva elektrona. Med seboj se ne odbijajo, ker se vrtijo v nasprotnih smereh in ustvarjajo magnetna polja, ki se privlačijo. Torej, sila privlačnosti, ki je magnetna; in odbojnost, ki je električna, je uravnotežena.

Nasproti ali antiparalelno se vrtijo, elektroni se vrtijo v nasprotnih smereh.
Tako v vsakem majhnem kvadratu predstavljamo največ dva elektrona, ki sta predstavljena s puščicami in imata vrednosti +1/2 in -1/2.
↑ |
Po dogovoru predstavlja elektron z negativnim spinom s = -1/2.
↓ |
Po dogovoru predstavlja elektron s pozitivnim spinom s = +1/2.
Kot primer poglejmo element helij, ki ima dva elektrona in samo en nivo energije; njegov simbol je: 2on
↑↓ |
Njegova simbolna predstavitev je podana z:
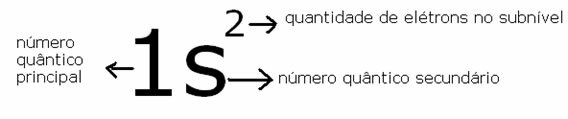
Prikaz položaja najbolj energičnega elektrona v heliju
Torej imamo njihova kvantna števila za 1. in 2. elektron:
1. elektron: 2. elektron:
n = 1 n = 1
l = 0 l = 0
m = 0 m = 0
s = -1/2 s = +1/2
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/numeros-quanticos-magnetico-m-ou-ml-spin-s-ou-ms.htm
