Ker je organskih spojin na tisoče, ima lahko pojav izomerije več oblik. Zato lahko izomerijo v osnovi razdelimo na dve vrsti: ploščata ali ustavna izomerija in vesoljska izomerija ali stereoizomerija. Vsak omenjeni tip je mogoče razdeliti, kot je prikazano na naslednjem diagramu:
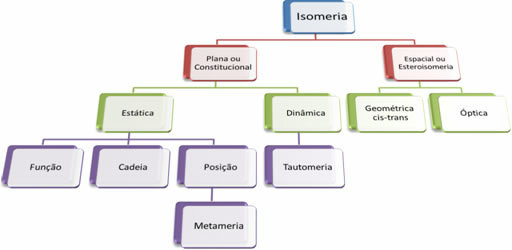
Glej vsak primer:
1. Ravna ali ustavna izomerija: Tovrstni izomeri imajo enako molekulsko formulo in jih ločimo s ploščatimi strukturnimi formulami. Obstaja pet primerov ravninske izomerije: funkcija, veriga, položaj, metamerizem in tavtomerija.
1.1.Funkcionalna ali funkcionalna izomerija: Razlika med izomeri je v funkcionalni skupini.
Primer: Molekulska formula C3H6O
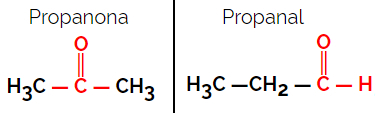
Upoštevajte, da je propanon iz ketonske skupine, propanal pa iz aldehidne skupine.
1.2. Verižni ali skeletni izomeri: Razlika med izomeri je v vrsti verige. Na primer, en izomer je odprte verige, drugi pa zaprte verige, ali eden je normalne verige, drugi pa razvejane verige, ali pa je ena homogena veriga, druga pa heterogena veriga.
Primer: Molekulska formula C4H10
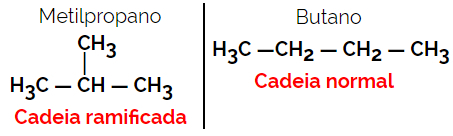
1.3.Pozicijska ali pozicijska izomerija: Razlika je v položaju nenasičene, funkcionalne skupine, heteroatoma ali substituenta.
Primer: Molekulska formula C4H6

1.4.Kompenzacijska izomerija ali metamerija: Gre za posebno vrsto izomerije položaja, kjer je razlika v položaju heteroatoma.
Primer: Molekulska formula C4H10O
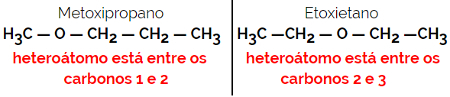
1.5.Dinamična izomerija ali tavtomerija: Gre za posebno vrsto izomerije funkcij, pri kateri izomeri sobivajo v dinamičnem ravnovesju v raztopini. Dve glavni vrsti tavtomerije sta med ketonom in enolom (ketoenolska bilanca) ter med aldehidom in enolom (aldoenolska bilanca).
Primer: Molekulska formula C3H6O
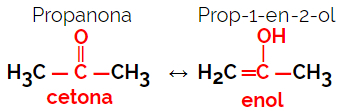
2. Vesoljska izomerija ali steroizomerija: V tem primeru je razliko med izomeri mogoče vizualizirati le skozi orientacijo njihovih atomov v prostoru. Obstajata dve vrsti stereoizomerije: geometrijska izomerija in optična izomerija.
2.1.Geometrijski ali cis-trans izomeri: Razlika je v tem, da je izomer, imenovan kot cis ima enake ogljikove ligande v dvojni vezi ali v cikličnih spojinah na isti strani ravnine. Izomerni ligandi trans so na nasprotnih straneh.
Primer: Molekulska formula C2H2Kl2

Te spojine se imenujejo stereoizomeri.
2.2.Optični izomer: Pojavi se, ko lahko izomeri odbijejo polariziran svetlobni žarek. Če upogne polariziran svetlobni žarek v levo, je levorotaren izomer, če pa se upogne v desno, se imenuje desnoruki izomer.
Primer:
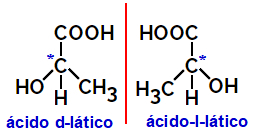
Asimetrične molekule, kot so zgoraj prikazane, ki so medsebojne zrcalne slike in jih ni mogoče prestaviti, se imenujejo enantiomeri.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm
