Reakcije oksidacije in redukcije, ki se pojavijo v prisotnosti vodikovega peroksida (vodna raztopina vodikovega peroksida - H2O2 (aq)) predstavljajo poseben primer, ki ga je treba analizirati ločeno, predvsem glede njegovega ravnotežja. To je zato, ker kisiki v vodikovem peroksidu, ki imajo Nox enak -1, lahko oksidirajo ali zmanjšajo.
Poglejmo si na primer dva primera, v katerih se najprej obnaša kot oksidacijsko sredstvo (reduciranje) in nato kot redukcijsko sredstvo (oksidacija):
- oksidacijsko sredstvo: kadarkoli se vodikov peroksid reducira in deluje kot oksidant, ustvari vodo kot produkt.
Če raztopini, ki vsebuje jodidne ione, dodamo raztopino vodikovega peroksida (I-) v kislem mediju bomo imeli:
H2O2 (aq) + Jaz-(tukaj) + H+(tukaj) → H2O(1) + Jaz2 (-i)
Glejte, da nastaneta voda in jod. Če pa želite preveriti, ali je vodikov peroksid dejansko deloval kot oksidacijsko sredstvo in se reduciral, upoštevajte določanje oksidacijskih števil (NOx): *

Vodikov peroksid kisika Nox se je zmanjšal z -1 na -2, saj je prejel 1 elektron. Ker pa imamo v vsaki molekuli vodikovega peroksida dva kisika (H
2O2), bo sprememba Noxa enaka 2.Torej, kot je prikazano v besedilu „Redox uravnoteženje", Je nujen korak za uravnoteženje reakcij z metodo oksidacijske redukcije pretvorba vrednosti variacij Nox s koeficienti, ki so v tem primeru naslednji:
* H2O2 = 2 (oxNox) = 2 → 2 bo koeficient I-;
* JAZ-= ∆Nox = 1 → 1 bo koeficient H2O2.
Tako imamo:
1 uro2O2 (aq) + 2 I-(tukaj) + H+(tukaj) → H2O(1) + Jaz2 (-i)
Doseganje ostalih koeficientov z uravnoteženjem po preskusih:
- Ker sta v 1. členu dva atoma kisika, mora biti koeficient vode v 2. členu enak 2. In ker sta v prvem članu tudi dva jodidna iona, bo jodni koeficient v drugem članu 1. Ne pozabite, da moramo indeks pomnožiti s koeficientom, da poiščemo pravilno količino atomov in ionov v vsakem članu:
1 uro2O2 (aq) + 2 I-(tukaj) + H+(tukaj) → 2 H2O(1) + 1 I2 (-i)
- Zdaj ostane samo uravnotežiti vodikov kation 1. člana in njegov koeficient bo moral biti enak 2, ker ima v 2. članu 4 vodike, v 1. članu pa že dva:
1 uro2O2 (aq) + 2 I-(tukaj) +2 H+(tukaj) → 2 H2O(1) + 1 I2 (-i)
- reduktor: kadar vodikov peroksid oksidira in deluje kot redukcijsko sredstvo, tvori kisik (O2) kot izdelek.
Primer zmanjšanja vodikovega peroksida je, ko pride v stik s kalijevim permanganatom (KMnO4). Ta snov ima zelo značilno vijolično barvo, vendar v stiku z vodikovim peroksidom postane brezbarvna. To je zato, ker je ves mangan prisoten v ionu MnO4- raztopine permanganata zmanjša, pri čemer nastane ion Mn2+, kot je prikazano spodaj:
+1 -1 +7 -2 +1 0 +2 +1 -2
H2O2 + MnO4-+ H+ → The2 + Mn2++ H2O
Pri izračunu Nox vidimo, da kisik v vodikovem peroksidu dejansko oksidira in povzroči zmanjšanje mangana:
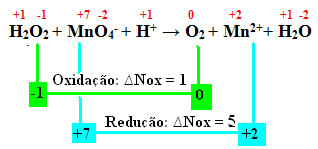
Kot v prejšnjem primeru bo tudi vrednost vodikovega peroksida enaka 2, saj sta dva kisika in vsak izgubi elektron. Zato imamo:
* O2 = 2 (oxNox) = 2 → 2 bo koeficient MnO4-;
* MnO4- = ∆Nox = 5 → 5 bo koeficient O2.
In kot vsi O2 izhaja iz vodikovega peroksida, imata dve snovi enak koeficient:
5 H2O2 + 2MnO4-+ H+ → 5 O2 + Mn2++ H2O
Izravnavo po poskusni metodi imamo:
5 ur2O2 + 2 MnO4-+ 6 H+ → 5 O.2 + 2 Mn2++ 8 H2O
* Za vsa vprašanja o izračunu oksidacijskega števila (Nox) atomov in ionov v reakciji preberite besedilo "Določanje oksidacijskega števila (Nox)".
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-envolvendo-agua-oxigenada.htm
