THE hasij, s simbolom Hs in atomsko število 108, je eden od elementov, znanih kot transaktinidi. Kot vsi elementi te skupine ga v naravi ne najdemo, ker je sintetičen, poleg tega je radioaktiven in nestabilen. Za njegovo sintezo so zaslužni nemški laboratoriji Helmholtzovega centra za raziskave težkih ionov (GSI) v mestu Darmstadium v Nemčiji, ime pa je dobilo v čast nemški deželi Hesse, ki se nahaja v osrednji regiji starši.
Hasij je najtežji element, katerega lastnosti so analizirane s poskusi, ki jih izvaja GSI sam. Rezultati so bili pomembni za potrditev položaja H v Periodični sistem, saj je bila zaznana podobnost med tem elementom in osmijem in rutenijem, lažjim elementoma skupine 8.
Preberite tudi:Bohrium - sintetični kemični element, imenovan po Nielsu Bohru
Hasijev povzetek
Je sintetični kemični element, ki se nahaja v skupini 8 periodnega sistema.
Sintetiziralo ga je Gesellschaft für Schwerionenforschung (GSI) v Darmstadiumu v Nemčiji.
Je radioaktivni element in nestabilen.
Teoretični in eksperimentalni podatki potrjujejo, da so njegove lastnosti podobne najlažjim elementom v svoji skupini.
Kot transaktinida ga ni mogoče proizvajati v velikem obsegu, razen s hitrostjo nekaj atomi.
Lastnosti hasija
simbol: hs
atomsko število: 108
atomska masa: 277 c.u.
Elektronska konfiguracija: [Rn] 7s2 5f14 6d6
Najbolj stabilen izotop: 269Hs (14 sekund razpolovni čas)
Kemična serija: skupina 8; transaktinidi; super težki elementi.
Lastnosti hasija
Hasij je a sintetični element in najtežji iz skupine 8. Šteje se za a transaktinid, prav zato, ker se pojavlja v periodnem sistemu po seriji aktinidov. Tako kot vsi transaktinidi je tudi hasij element radioaktivno in nestabilno.
To pomeni, da njeni izotopi dosežejo malo časa polovično življenje (čas, potreben, da se masa atomske vrste zmanjša za polovico). Trenutno je znanih sedem izotopov hasija, katerih masa variira od 264 a.m.u. do 270. a.m.u. Med vsemi je najbolj stabilen izotop 269Hs, z razpolovno dobo 14 sekund.
Čeprav kratka razpolovna doba otežuje preučevanje kemičnih lastnosti transaktinidov, je imel hasij v tem pogledu nekoliko več sreče. Junija 2001 je bilo objavljeno, da je postal najtežji element, za katerega so analizirane njegove lastnosti.
Ekipi je v mestu Darmstádio v Nemčiji uspelo proizvesti približno šest atomov Hs z razpolovno dobo približno 10 sekund. Čeprav se zdi malo, je bilo to dovolj za potrditev, da ima hasijev oksid HsO4, ima močno podobnost z oksidi lažjih elementov skupine 8, RuO4 in OsO4, to je rutenij to je osmij.
Glej tudi: Seaborgium je še en sintetični kemični element z radioaktivnimi lastnostmi in kratko razpolovno dobo
Pridobivanje Hasija
Transaktinidom je skupna težava pri proizvodnji. Na splošno je potrebna najsodobnejša oprema, kot npr pospeševalniki delcev. V teh ionske vrste trčijo z elementi visoke atomska masa za tvorbo supertežkih elementov (v katere je vključen Hs).
V primeru hasija so študije, ki so potrdile njegov položaj v skupini 8 periodične tabele, vključevale njegovo proizvodnjo z bombardiranjem magnezija-26, pri čemer je bil cilj kurij-248.
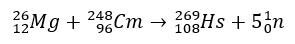
Poskusi, ki vključujejo te elemente, so dragi, zato je običajno, da se izvajajo teoretične študije, natančno za izračun in napovedovanje kemijskih lastnosti. Kratka razpolovna doba je še en zapleten dejavnik.
Eksperimentalne tehnike oz ločitev in odkrivanje mora biti zelo hiter, da se dosežejo verodostojni rezultati. Končno je reakcijska učinkovitost teh elementov zelo nizka in je v območju nekaj atomskih enot.
Previdnostni ukrepi pri uporabi Hasija
Hs se ne proizvaja v velikem obsegu, zato se z njim manipulira ne vključuje tveganj. Poleg tega ga pridobivajo v raziskovalnih centrih z zelo nadzorovanimi okolji.
zgodovina hasija

Transaktinidi so bili protagonisti znanstvenega spora zaradi Hladna vojna, a Vojna prenosov, ime, ustvarjeno glede na spore, ki so vključevali proizvodnjo in prepoznavanje elementov po fermiju (Fm, Z = 100). V tej dirki so sodelovali laboratoriji:
Skupni inštitut za jedrske raziskave v mestu Dubna v Rusiji;
Lawrence Berkeley National Laboratory v Berkeleyju v Kaliforniji;
Gesellschaft für Schwerionenforschung (GSI, bolje prevedeno kot Helmholtzov center za raziskave težkih ionov) v Darmstadiumu v Nemčiji.
V primeru elementa 108 sta bili vključeni skupini GSI in Dubna. Čeprav so znanstveniki iz Dubne (voditelj Yuri Oganessian) prvi poročali o prisotnosti elementa 108, so zasluge vzeli tisti iz nemške skupine, saj GSI je predstavil prepričljivejše rezultate, medtem ko mu je v enem poskusu uspelo proizvesti tri atome izotopa 265, v drugem pa en atom izotopa 264.
Ti izotopi so bili proizvedeni z uporabo univerzalnega linearnega pospeševalnika (Unilac, bolje prevedeno kot univerzalni linearni pospeševalnik), z bombardiranjem 208Pb po 58vera. Leta 1997 je Mednarodna zveza za čisto in uporabno kemijo (IUPAC) prepoznala element 108 s simbolom Hs, kot Hasija v čast nemške dežele Hesse.
Rešene vaje na hasiju
Vprašanje 1
Hasij, simbol Hs, velja za najtežji element, katerega lastnosti so eksperimentalno preučene. Takrat so raziskovalci lahko določili lastnosti hazijevega tetroksida, HsO4. Pri tej vrsti ima Hs enak NOx kot lažja elementa svoje skupine, osmij (Os) in rutenij (Ru). Oksidacijsko število Hs v hazijevem tetroksidu je enako:
a) 0
B) +2
C) +4
D) +6
E) +8
Resolucija:
Alternativa E
THE kisik, ko v a oksid, pridobi naboj enak -2. Torej NOx od Hs, ki ga bomo imenovali x, lahko izračunamo kot:
x + 4(-2) = 0
x - 8 = 0
x = +8
vprašanje 2
Najstabilnejši izotop hasija, Hs, ima razpolovno dobo le 14 sekund. To pomeni:
A) v 14 sekundah se bo masa izotopa Hs podvojila.
B) po 14 sekundah bo masa izotopa Hs manjša od polovice začetne mase.
C) čez nekaj manj kot minuto bo masa izotopa Hs 1/16 njegove začetne mase.
D) v eni minuti bo masa izotopa Hs natanko polovica njegove začetne mase.
E) v 14 sekundah bo masa izotopa Hs deljena s 4.
Resolucija:
Alternativa C
Razpolovna doba označuje čas, potreben, da se količina atomske vrste prepolovi. To pomeni, da se vsakih 14 sekund količina Hs zmanjša za polovico. Z opazovanjem te razpolovne dobe je jasno, da so bile s 56 sekundami že dosežene štiri razpolovne dobe, zaradi česar je masa Hs deljena z 24, kar je 16.
Avtor: Stefano Araújo Novais
Učiteljica kemije