Pri oksidacijske reakcije s sekundarnimi alkoholi so tiste, pri katerih je interakcija med organsko spojino iz skupine alkoholi, ki mora biti sekundarni, in tako imenovani Bayerjev reagent (KMnO4) v kislem mediju.
Kadarkoli je Bayerjev reagent v kislem mediju (aq/H+), je podvržen reakciji razgradnje, pri čemer nastanejo kalijev oksid, manganov oksid II in nastajajoči kisiki, kot lahko vidimo v naslednji enačbi:
2 kmnO4 (vodni/H+) → 2 MnO + K2O + 5 [O]
V kateri koli oksidacijski reakciji je nastajajočih kisikov, ki izvira iz razgradnje kalijevega permanganata v kislem mediju, napada ogljikove verige ki imajo pi vezi med ogljiki (alkeni, alkini in alkadieni) ali so zaprti (ciklani, aromatski cikleni), pri čemer nastajajo nove kemične spojine.
V primeru oksidacijska reakcija v sekundarnih alkoholih, preden razumemo reakcijski mehanizem, se je treba spomniti koncepta sekundarnega alkohola. je poklican sekundarni alkohol tisti, v katerem je hidroksil (OH) vezan na a sekundarni ogljik (ogljik vezan neposredno na dva druga ogljikova atoma). Oglejte si prikaz sekundarnega alkohola:
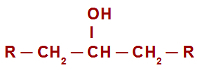
Splošna strukturna formula sekundarnega alkohola
V vsaki oksidacijski reakciji v alkoholih nastajajoči kisiki napadejo vodike, ki se nahajajo na ogljiku, ki ima hidroksilno skupino. V primeru oksidacijskih reakcij v sekundarnih alkoholih imajo kisiki samo en atom vodika za napad v vsaki strukturi te vrste alkohola.
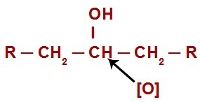
Nastajajoči kisik, ki napada sekundarni alkohol
Ko napade vodik (H), prisoten v hidroksilnem ogljiku (OH), nastajajoči kisik ([O]) tvori nov hidroksil na istem ogljiku. Torej imamo gemino diola v zaporu. Ker je gemino diol (HO – C – OH) nestabilen, se razgradi v molekulo vode.Vendar pa med ogljikom in kisikom, ki ostaneta od enega od hidroksilov, nastane dvojna vez (pi in sigma).
Ne nehaj zdaj... Po reklami je še več ;)
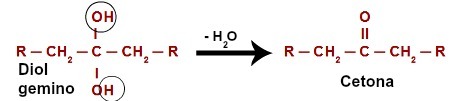
Kemična enačba oksidacije sekundarnega alkohola
Produkt, ki nastane pri oksidacijski reakciji sekundarnih alkoholov, je vedno a keton, saj dvojna vez vedno nastane pri sekundarnem ogljiku, kar povzroči karbonil med dvema ogljikoma in tako tvori keton.
Glej zdaj a Primer oksidacijske reakcije v sekundarnih alkoholih.
Primer: Butan-2-ol
O butan-2-ol je sekundarni alkohol, saj je hidroksil vezan na sekundarni ogljikov atom. Torej, na ogljiku, ki ima hidroksil, je samo en vodik. To dejstvo lahko preverimo v spodnji strukturi:

Ko je izpostavljen mediju, ki vsebuje vodo, kislino in KMnO4 (Bayerjev reagent), vaš vodik napade nastajajoči kisik, ki se preoblikuje v nov hidroksil, kar povzroči gemino diol.

Končno pride do razgradnje dveh hidroksil, prisotnih v gemino diolu, tako nastane molekula vode in keton, zaradi potrebe po ustvarjanju vezi med ogljikom in enim od kisikov razpadlih hidroksilov.

lahko predstavljamo celotno reakcijo oksidacije butan-2-ola z naslednjo enačbo:

Jaz, Diogo Lopes Dias
Ali se želite sklicevati na to besedilo v šolskem ali akademskem delu? Poglej:
DNI, Diogo Lopes. "Oksidacijske reakcije v sekundarnih alkoholih"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/reacoes-oxidacao-alcoois-secundarios.htm. Dostop 27. julija 2021.
Kemija

Hidroksilna funkcionalna skupina, primarni alkoholi, sekundarni alkoholi, terciarni alkoholi, metanol, glicerol, etanol, priprava nitroglicerina, proizvodnja barv, proizvodnja alkoholnih pijač, ocetne kisline, goriva za avtomobili.



