Nitrati so anorganske spojine, ki vsebujejo anion NO3-.
Dušik je družina 15, ima 5 elektronov v valenčni lupini in mora ustvariti tri kovalentne vezi (s skupnimi elektroni) imeti osem elektronov v valenčni lupini in tako imeti stabilen. Vendar ima vsak kisik 6 elektronov v zadnji lupini in zato mora vsak njegov atom ustvariti dve vezi, da je stabilen.
Torej, v nitratnem anionu je dušik osrednji element, ki tvori dvojno vez z enim od kisikov, ki je stabilna, enojna vez z enim od drugih dveh kisikov, z drugim pa kovalentna vez dativ. To pomeni, da eden od kisikov ni stabilen in mora prejeti še 1 elektron, kar daje skupni naboj enak -1. Z dativnim dušikom naredi vez več, kot bi lahko naredil, dari enega od svojih elektronov in dobi naboj, enak +1. Spodaj si oglejte strukturo tega aniona:
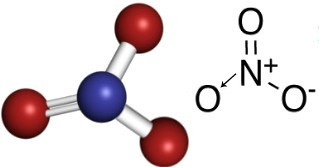
Ta anion lahko sprejme elektron in tvori električno nevtralno spojino, anorgansko sol. Vse te spojine so topne v vodi.
Glavna uporaba nitratov je v zdravilih, kot so vazodilatatorji pri zdravljenju angine pektoris (bolečine v posledica nizke oskrbe s kisikom zaradi pretoka krvi v srčno mišico) in erektilne disfunkcije moški. Uporabljajo se tudi v gnojilih in eksplozivih, kot bo omenjeno kasneje.
Nitrate lahko proizvedemo z reakcijo nevtralizacije dušikove kisline (HNO).3) z neko osnovo. Glejte spodnji primer, kjer je nastal magnezijev nitrat:
HNO3 + Mg(OH)2 → Mg (ŠT3)2+ H2O
Trije glavni primeri te vrste spojin so natrijev nitrat (NaNO3), kalijev nitrat (KNO3) in amonijev nitrat (NH4PRI3). V vseh teh primerih so kationi (Na+,K+ in NH4+) zagotovijo 1 elektron nitratnemu anionu. Toda v resnici se ti nasprotni naboji privlačijo drug drugega in tvorijo dobro opredeljene ionske grozde, ki so kristalne mreže. Tako so nitrati običajno kristalne trdne snovi, kot je prikazano spodaj v primeru natrijevega nitrata:
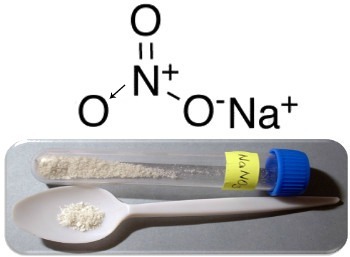
Ta spojina se uporablja pri proizvodnji gnojil, znana pa je predvsem kot Čilska salitra, saj so v čilskih puščavah njegova velika nahajališča. Preoblikuje se v kalijev nitrat, ki se uporablja za izdelavo črnega smodnika, ki se uporablja v različnih orožjih in eksplozivih.

Tako natrijev kot kalijev nitrat se imenujeta "solitra" in se pogosto uporabljata kot konzervansi barve konzerviranega in prekajenega mesa, pa tudi v nekaterih živilih za večji občutek sitosti. Vendar pa njegovo uživanje resno škoduje zdravju, saj lahko te nitrate pretvorijo bakterije iz organizem v nitrite in pozneje v nitrozamine, ki so rakotvorni in povzročajo predvsem raka v želodec. Nitriti tudi pretvarjajo hemoglobine v krvi, zaradi česar ne morejo prenašati kisika.
Glavni vzroki prekomernega vnosa nitratov so uporaba dušikovih gnojil pri pridelavi zelenjave.
Saltitra je nevarna tudi zato, ker poveča koncentracijo natrijevih ionov v telesu, kar lahko povzroči težave s srcem, kot je visok krvni tlak.
O amonijev nitrat uporablja se tudi kot gnojilo in eksploziv, uporabljen pa je bil celo s kurilnim oljem v terorističnem napadu na zgradbe Svetovnega trgovinskega centra 11. septembra 2001.

V napadu na Svetovni trgovinski center je bil uporabljen amonijev nitrat*
* Avtorske pravice za sliko: Dan Howell in Shutterstock.com
Avtor: Jennifer Fogaça
Diplomirala iz kemije
