O uravnoteženje enačb nam omogoča, da primerjamo število atomov, prisotnih v kemijski enačbi, tako da postane resnična in predstavlja kemično reakcijo.
Uporabite spodnja vprašanja, da preizkusite svoje znanje in preverite odgovore, komentirane po povratnih informacijah, da odgovorite na svoja vprašanja.
Vprašanje 1
(Mackenzie-SP)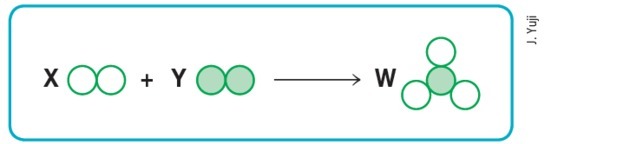
Ob predpostavki, da prazni in napolnjeni krogi pomenijo različne atome, potem shema zgoraj bo predstavljalo uravnoteženo kemijsko reakcijo, če bomo črke X, Y in W zamenjali z vrednote:
a) 1, 2 in 3.
b) 1, 2 in 2.
c) 2, 1 in 3.
d) 3, 1 in 2.
e) 3, 2 in 2.
Alternativa d) 3, 1 in 2.
1. korak: Za lažje razumevanje enačbe dodelimo črke.
2. korak: dodajamo indekse, da vemo, kdo ima v enačbi največ atomov.
| THE | |
| B |
A in B se v vsakem članu enačbe pojavita le enkrat. Če pa seštejemo indekse, vidimo, da ima A najvišjo vrednost. Zato smo zanj začeli izravnavo.
3. korak: Element A uravnotežimo tako, da indekse prenesemo in jih spremenimo v koeficiente.
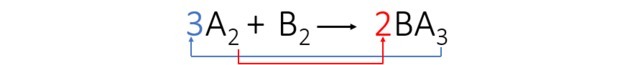
Opazili smo, da je bil element B samodejno uravnotežen, koeficienti enačbe pa so: 3, 1 in 2.
2. vprašanje
(Unicamp-SP) Preberite naslednji stavek in ga s simboli in formulami pretvorite v (uravnoteženo) kemijsko enačbo: „molekula plinastega dušika, ki vsebuje dva atoma dušik na molekulo, reagira s tremi molekulami dvoatomskega, plinastega vodika, pri čemer nastane dve molekuli plinastega amoniaka, ki je sestavljen iz treh atomov vodika in enega od dušik ".
Odgovor:
Če predstavljamo atome, opisane v vprašanju, lahko razumemo, da se reakcija pojavi na naslednji način:
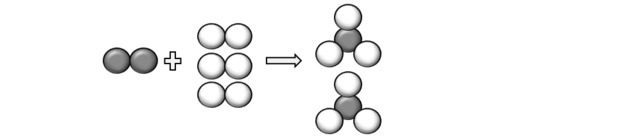
Torej pridemo do enačbe:
3. vprašanje
Vodikov peroksid je kemična spojina, ki se lahko razgradi in tvori vodo in kisik, v skladu s spodnjo kemijsko enačbo.
Glede te reakcije je pravilno uravnotežena enačba:
a) H2O2 → The2 + H2O
b) 2 uri2O2 → The2 + 2H2O
c) H2O2 → 2O2 + H2O
d) 2 uri2O2 → 2O2 + 2H2O
Pravilna alternativa: b) 2H2O2 → The2 + 2H2O
Upoštevajte, da je vodikov peroksid kemikalija, sestavljena iz atomov dveh kemičnih elementov: vodika in kisika.
Po reakciji razgradnje morate imeti v reaktantih in produktih enako število atomov obeh elementov. Za to moramo uravnotežiti enačbo.
Upoštevajte, da imamo v reaktantu 2 atoma vodika (H2O2) in dva atoma v izdelku (H2O). Vendar ima kisik v reaktantu dva atoma (H2O2) in trije atomi v izdelkih (H2O in O2).
Če postavimo koeficient 2 pred vodikov peroksid, podvojimo število atomov v elementih.
Upoštevajte, da če enak koeficient damo skupaj s formulo za vodo, imamo na obeh straneh enako količino atomov.
Zato je pravilno uravnotežena kemijska enačba 2H2O2 → The2 + 2H2O.
4. vprašanje
(UFPE) Upoštevajte spodnje kemijske reakcije.
Lahko rečemo, da:
a) vsi so uravnoteženi.
b) 2, 3 in 4 so uravnoteženi.
c) uravnoteženi sta le 2 in 4.
d) samo 1 je neuravnotežen.
e) nobena ni pravilno uravnotežena, ker so agregatna stanja reaktantov in produktov različna.
Alternativa b) 2, 3 in 4 so uravnotežene.
Alternativa 1 in 5 sta napačni, ker:
- Enačba 1 je neuravnotežena, pravilno stanje bi bilo:
- Enačba 5 ni pravilna, ker bi bila spojina, ki nastane v reakciji, H2SAMO3.
Za oblikovanje H2SAMO4 je treba v enačbo vključiti oksidacijo SO2.
5. vprašanje
(Mackenzie-SP) Segret na 800 ° C kalcijev karbonat razpade v kalcijev oksid (deviško apno) in ogljikov dioksid. Pravilno uravnotežena enačba, ki ustreza opisanemu pojavu, je:
(Podano: Ca - zemeljskoalkalijska kovina.)
Alternativa c)
Kalcij je zemeljskoalkalijska kovina in za stabilnost kalcija potrebuje 2 elektrona (Ca2+), ki je naboj kisika (O2-).
Tako se atom kalcija veže na atom kisika in nastala spojina je CaO, ki je živo apno.
Drugi izdelek je ogljikov dioksid (CO2). Oba tvorita kalcijev karbonat (CaCO3).
Če ga postavimo v enačbo:
Upoštevamo, da so količine atomov že pravilne in jih ni treba uravnotežiti.
6. vprašanje
(UFMG) Enačba ni uravnoteženo. Če ga uravnotežimo z najmanjšimi možnimi števili, bo vsota stehiometričnih koeficientov:
a) 4
b) 7
c) 10
d) 11
e) 12.
Alternativa e) 12
Z uporabo preskusne metode bo vrstni red izravnave:
1. korak: Ker je element, ki se v vsakem članu pojavi le enkrat in ima najvišji indeks, kalcij, smo ga začeli uravnotežiti.
2. korak: Sledimo uravnoteženju s strani radikalnega PO43-, ki se prav tako pojavi le enkrat.
3. korak: uravnotežimo vodik.
S tem opažamo, da se je samodejno prilagodila količina kisika in ravnotežje enačbe je:
Če se spomnite, da ko je koeficient 1, vam tega ni treba zapisati v enačbo.
Če dodamo koeficiente, ki jih imamo:
7. vprašanje
Zgorevanje je vrsta kemične reakcije, pri kateri se energija sprošča v obliki toplote.
Pri popolnem zgorevanju snovi, ki jo tvorita ogljik in vodik, nastaneta ogljikov dioksid in voda.
Opazujte reakcije izgorevanja ogljikovodikov in odgovorite, katera od spodnjih enačb je napačno uravnotežena:
a) CH4 + 2O2 → CO2 + 2H2O
b) C.3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
d) C.2H6 + 7 / 2O2 → 2CO2 + 3H2O
Nepravilen odgovor: c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
Za uravnoteženje kemijskih enačb najprej poglejmo, kateri element se pojavi samo enkrat v vsakem članu enačbe.
Upoštevajte, da ogljik in vodik tvorita samo en reagent in en produkt v vsaki predstavljeni enačbi.
Začnimo torej z uravnoteženjem z vodikom, saj ima večje število atomov.
Zato bo vrstni red uravnoteženja:
- Vodik
- Ogljik
- Kisik
Vodik
Ker ima izdelek dva atoma vodika, vstavimo število kot koeficient, ki pomnoženo z 2 povzroči število atomov vodika v reaktantu.
a) CH4 + O2 → CO2 + 2H2O
b) C.3H8 + O2 → CO2 + 4H2O
c) C4H10 + O2 → CO2 + 5H2O
d) C.2H6 + O2 → CO2 + 3H2O
Ogljik
Izravnava se izvede tako, da se indeks ogljika v reaktantu prenese in uporabi kot koeficient na izdelku, ki ima atome tega elementa.
a) CH4 + O2 → 1CO2 + 2H2O
b) C.3H8 + O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
d) C.2H6 + O2 → 2CO2 + 3H2O
Kisik
Če seštejemo število atomov kisika v nastalih produktih, najdemo število atomov elementa, ki mora reagirati.
Za to moramo kot koeficient postaviti število, ki pomnoženo z 2 povzroči število atomov kisika v izdelkih.
a) CH4 + O2 → 1CO2 + 2H2O
2x = 2 + 2
2x = 4
x = 2
Torej pravilna enačba je: CH4 + 2O2 → 1CO2 + 2H2O.
b) C.3H8 + O2 → 3CO2 + 4H2O
2x = 6 + 4
2x = 10
x = 5
Torej pravilna enačba je: C3H8 + 5O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
2x = 8 + 5
2x = 13
x = 13/2
Torej pravilna enačba je: C4H10 + 13/2O2 → 4CO2+ 5h2O
d) C.2H6 + O2 → 2CO2 + 3H2O
2x = 4 + 3
2x = 7
x = 7/2
Torej pravilna enačba je: C2H6 + 7/2O2 → 2CO2 + 3H2O
Pravilno uravnotežene enačbe so:
a) CH4 + 2O2 → CO2 + 2H2O
b) C.3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 2O2 → 4CO2 + 5h2O
d) C.2H6 + 7 / 2O2 → 2CO2 + 3H2O
Torej, alternativa c) C4H10 + 13 / 3O2 → 4CO2 + 5h2Stvar je v tem, da nima pravega ravnotežja.
vprašanje 8
(Enem 2015) Apnenci so materiali, sestavljeni iz kalcijevega karbonata, ki lahko delujejo kot sorbenti za žveplov dioksid (SO2), pomembno onesnaževalo zraka. Reakcije, ki sodelujejo v procesu, so aktivacija apnenca s kalcinacijo in fiksacija SO2 s tvorbo kalcijeve soli, kar ponazarjajo poenostavljene kemijske enačbe.
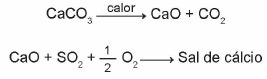
Glede na reakcije, ki sodelujejo pri tem postopku razžvepljevanja, kemična formula kalcijeve soli ustreza:
Alternativa b)
Ker je reakcija uravnotežena, morajo biti atomi v reaktantih v proizvodih v enaki količini. Tako
Nastala sol je sestavljena iz:
1 atom kalcija = Ca
1 atom žvepla = S
4 atomi kisika = O4
Zato kemijska formula kalcijeve soli ustreza CaSO4.
9. vprašanje
(UFPI) Spodaj je prikazana reakcija X z Y. Ugotovite, katera enačba najbolje predstavlja uravnoteženo kemijsko enačbo.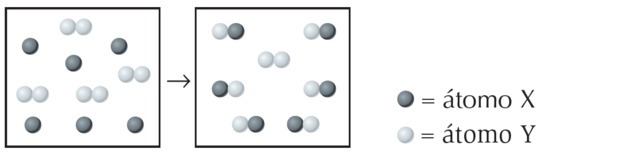
Alternativa a)
Na sliki opažamo, da je vrsta X en sam atom, medtem ko je Y dvoatomska, to je, da nastane s spajanjem 2 atomov. Torej X reagira z Y2.
Nastali izdelek predstavlja XY, enačba pa je neuravnotežena:
Enačbo uravnotežimo na naslednji način:
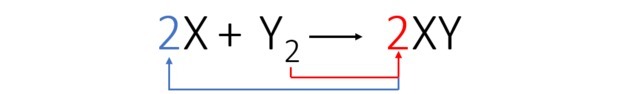
Glede na uravnoteženo enačbo nam spodnja slika prikazuje, kako pride do reakcije in njen delež.
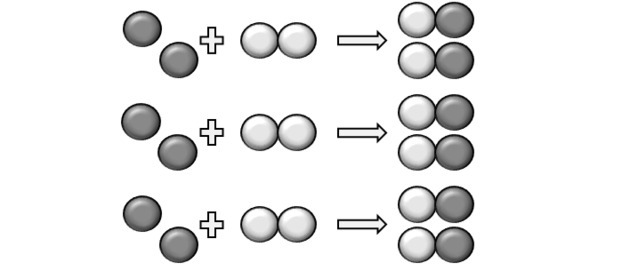
Da lahko pride do reakcije, mora biti določeno razmerje, zato nekatera spojina morda ne bo reagirala. To prikazuje slika, saj v izdelku vidimo, da je Y2 ni reagiral.
10. vprašanje
(Enem 2010) Mobilizacije za promocijo boljšega planeta za prihodnje generacije so vse pogostejše. Večino množičnih prevoznih sredstev trenutno poganja fosilno gorivo. Kot primer obremenitve, ki jo povzroča ta praksa, je dovolj, da vemo, da avtomobil v povprečju proizvede približno 200 g ogljikovega dioksida na prevoženi kilometer.
Revija za globalno segrevanje. 2., 8. leto. Objava Instituto Brasileiro de Cultura Ltda.
Ena glavnih sestavin bencina je oktan (C8H18). Z izgorevanjem oktanske energije je možno, kar omogoča, da se avto začne premikati. Enačba, ki predstavlja kemično reakcijo tega postopka, dokazuje, da:
a) pri tem se sprosti kisik v obliki O2.
b) stehiometrični koeficient za vodo je 8 do 1 oktan.
c) v procesu pride do porabe vode, tako da se energija sprosti.
d) stehiometrični koeficient za kisik je 12,5 do 1 oktan.
e) stehiometrični koeficient za ogljikov dioksid je 9 do 1 oktan
D) stehiometrični koeficient za kisik je 12,5 do 1 oktan.
Pri uravnoteženju enačbe najdemo naslednje koeficiente:
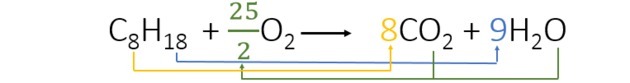
- Začeli smo z uravnoteženjem z vodikom, ki se pojavi samo enkrat v vsakem članu in ima višji indeks. Ker je 18 reakcijskih atomov vodika, sta v izdelku 2, zato moramo dodati število, pomnoženo z 2, da 18. Torej 9 je koeficient.
- Nato pred CO dodamo koeficient 82 imeti 8 ogljikov v vsakem članu enačbe.
- Na koncu dodajte količino kisika v izdelek in poiščite vrednost, pomnoženo z 2, kar nam da 25 atomov kisika. Tako smo izbrali 25/2 ali 12,5.
Tako se za zgorevanje 1 oktana porabi 12,5 kisika.
vprašanje 11
(Fatec-SP) Bistvena značilnost gnojil je njihova topnost v vodi. Zato industrija gnojil pretvori kalcijev fosfat, katerega topnost v vodi je zelo nizka, v veliko bolj topno spojino, ki je kalcijev superfosfat. Ta postopek predstavlja enačba:
kjer so vrednosti x, y oziroma z:
a) 4, 2 in 2.
b) 3, 6 in 3.
c) 2, 2 in 2.
d) 5, 2 in 3.
e) 3, 2 in 2.
Alternativa e) 3, 2 in 2.
Z uporabo algebraične metode oblikujemo enačbe za vsak element in enačimo število atomov v reaktantu s številom atomov v izdelku. Zato:
Uravnotežena enačba:
vprašanje 12
Spodnje enačbe uravnotežite s poskusno metodo.
Odgovor:
Enačbo sestavljata elementa vodik in klor. Elemente uravnotežimo samo tako, da pred izdelek dodamo koeficient 2.
Enačbe ni bilo treba uravnotežiti, saj so količine atomov že prilagojene.
Fosfor ima dva atoma v reaktantih, zato za uravnoteženje tega elementa prilagodimo količino fosforne kisline v izdelku na 2H3PRAH4.
Po tem smo opazili, da ima vodik v izdelku 6 atomov, uravnotežili smo količino tega elementa in dodali koeficient 3 reaktantu, ki ga vsebuje.
S prejšnjimi koraki je bila količina kisika določena.
Če pogledamo enačbo, vidimo, da so količine vodika in broma v izdelkih dvojne če je v reagentih, torej HBr dodamo koeficient 2, da uravnotežimo ta dva elementi.
Klor ima v proizvodih 3 atome in v reaktantih le 1 atom, zato uravnotežimo, tako da pred HCl damo koeficient 3.
Vodik je imel 3 atome v reaktantih in 2 atoma v produktih. Za prilagoditev količin pretvorimo indeks H2 v koeficientu pomnožimo s 3, ki je bil že v HCl, in dobimo rezultat 6HCl.
Količine klora v izdelkih prilagodimo tako, da imajo tudi 6 atomov in dobimo 2AlCl3.
Aluminij je imel v izdelkih 2 atoma, količino v reaktantih smo prilagodili na 2Al.
Količino vodika v izdelku uravnotežimo s 3H2 in prilagodimo količino 6 atomov tega elementa v vsak člen enačbe.
V enačbi je nitratni radikal (NO3-) ima v izdelku indeks 2, pretvorimo indeks v koeficient v reaktantu za 2AgNO3.
Količino srebra je bilo treba prilagoditi, saj ima zdaj v reagentih 2 atoma, zato imamo v izdelku 2Ag.
V reaktantih imamo 4 atome vodika in za uravnoteženje tega elementa produktu HCl dodamo koeficient 2.
Klor ima zdaj v izdelkih 4 atome, zato količino reagenta prilagodimo na 2Cl2.
V reagentih imamo 6 atomov vodika in za uravnoteženje tega elementa prilagodimo količino vode na 3H2O.
V reagentih imamo 2 ogljikova atoma in za uravnoteženje tega elementa prilagodimo količino ogljikovega dioksida na 2CO2.
Kisik mora imeti v reaktantih 7 atomov in za uravnoteženje tega elementa prilagodimo količino molekularnega kisika na 3O2.
Če pogledamo enačbo, nitratni radikal (NO3-) ima v izdelku indeks 2. Indeks pretvorimo v koeficient 2 v reagentu AgNO3.
V reagentih imamo 2 atoma srebra in za uravnoteženje tega elementa prilagodimo količino srebrovega klorida v izdelku na 2AgCl.
V izdelku imamo 3 atome kalcija in za uravnoteženje tega elementa prilagodimo količino kalcijevega nitrata v reagentu na 3Ca (NO3)2.
Nato nam ostane 6 NO radikalov3- v reaktantih in za uravnoteženje tega radikala prilagodimo količino dušikove kisline v proizvodih na 6HNO3.
Zdaj imamo v izdelkih 6 atomov vodika in za uravnoteženje tega elementa prilagodimo količino fosforne kisline v reagentu na 2H3PRAH4.
Več o izračunih s kemičnimi enačbami preberite na:
- Uravnavanje kemijskih enačb
- Stehiometrija
- Stehiometrični izračuni
- Vaje za stehiometrijo
- Vaje v periodnem sistemu