Celice ali baterije, katerih glavna sestavina je litij, imajo kot eno od značilnosti dejstvo, da so zelo lahke, saj je litij doslej odkrita najmanj gosta kovina. Da bi dobili idejo, ta srebrno bela kovina plava v vodi, saj je dvakrat gostejša kot je. To je posledica dejstva, da ima litij le tri protone in tri nevtrone.
Obstajata dve glavni vrsti litijevih baterij, od katerih se ena imenuje litij jod baterija. Razvit je bil predvsem za uporabo v srčni spodbujevalniki, ker je zelo lahek, varen (ne sprošča plinov, saj je hermetično zaprt), ima dober vzdržljivost (približno 8 do 10 let), zagotavlja napetost 2,8 V in visoko gostoto naboja (0,8 Wh / cm3).
Elektrode tvorita litij in jodov kompleks, ki sta ločena s kristalno plastjo litijevega jodida, ki omogoča prehod električnega toka. O kovinski litij deluje kot anoda te celice, to je negativni pol, ki oksidira in izgubi elektrone. že katoda, pozitivni pol, ki zmanjšuje, sprejema elektrone, je jodni kompleks.
Oglejte si polreakcije, ki se pojavijo v elektrodah, in enačbo, ki predstavlja globalno reakcijo te vrste celic:
Anodna polovična reakcija: 2 Li(s) → 2 Prebral sem+(s) + 2e-
Pol reakcija katode: 1 I2 (-i) + 2e-→ 2 I-(s)
Globalna reakcija: 2 Li(s) + 1 I2 (-i) → 2 LiI(s)
Litij-jodove baterije so v obliki zelo majhnih kovancev, kot je prikazano na spodnji sliki:

Druga vrsta celic ali baterij je litijev ion. To ime ima točno zato, ker njegovo delovanje temelji na gibanju litijevih ionov (Li+). Trenutno se pogosto uporablja v baterije za mobilni telefon njegov potencial pa se giblje med 3,0 in 3,5 V.

Anodo in katodo tvorijo atomi, razporejeni v ravninah, kot so plošče s prostori, v katere so vstavljeni litijevi ioni. O anoda tvori grafit s kovino bakra in ioni se interkalirajo v ravninah šesterokotne ogljikove strukture in tvorijo naslednjo snov: preberiteyÇ6. že katoda tvorijo litijevi ioni, interkalirani v oksid z lamelarno strukturo (preberitexCoO2).
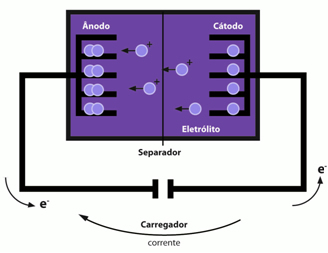
Tako imamo, da litijevi ioni zapustijo anodo in migrirajo skozi nevodno topilo na katodo.
Anodna polovična reakcija: LiyÇ6 (s) → y Li + Ç6+y-
Katodna polreakcija: LixCoO2 (-i) + y preberite+(s) + y in- → Prebrala semx + yCoO2 (-i)
Globalna reakcija: LiyÇ6 (s) + preberixCoO2 → Ç6(s) +preberitex + yCoO2 (-i)
Te baterije je mogoče polniti, preprosto z uporabo zunanjega električnega toka, ki povzroči migracijo litijevih ionov v nasprotno smer, to je iz oksida v grafit.

Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/pilhas-baterias-litio.htm
