Benzen je aromatski ogljikovodik, katerega formula je C6H6.
Je brezbarvna tekoča spojina z značilnim sladkim vonjem in zelo strupena. Vdihavanje benzena lahko povzroči resne zdravstvene težave.
Vsi aromatski ogljikovodiki imajo benzen ali aromatske obroče.
Lastnosti
Benzen je leta 1825 odkril znanstvenik Michael Faraday (1791-1867).
Znanstveniki že dolgo poskušajo razumeti strukturo benzena.
Šele leta 1865 je kemik Kekulé (1829-1896) predlagal obliko šesterokotnega obroča s parom uravnotežene strukture in izmeničnimi dvojnimi vezmi.
Zmožnost elektronskega premikanja ali premestitve daje benzenu aromatičen značaj.
Druge pomembne značilnosti benzena so:
- Šesterokotna in zaprta struktura.
- Sestavljen je iz šestih atomov ogljika, ki so enakovredni in enako oddaljeni. To je zato, ker so njihovi monosubstituirani derivati v celoti enaki.
- Njegovi disubstituirani derivati izhajajo iz treh različnih izomerov.
Benzen je mogoče predstaviti v naslednjih treh strukturah:
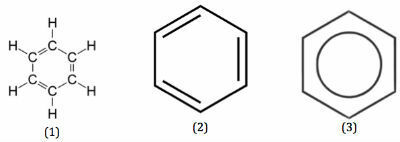
Preberite več o Aromatski ogljikovodiki.
Uporabe in toksičnost
Benzen je aromatski ogljikovodik, prisoten v Nafta, v bencinu in cigaretnem dimu. Najdemo ga tudi v vulkanih in gozdnih požarih.
V industriji in laboratorijih se uporablja kot topilo in je pomembna surovina za izdelavo drugih izdelkov.
Kljub pomembnosti na kemijskem in industrijskem področju je benzen zelo škodljiv za ljudi.
Vdihavanje benzena je glavna oblika zastrupitve. V kratkem obdobju lahko povzroči tresenje, zaspanost, pospešen srčni utrip in nezavest.
Že zaužitje hrane, onesnažene z benzenom, lahko privede do smrti.
Tudi benzen velja za rakotvorno snov.
Več o tem, lhej tudi:
- Ogljikovodiki
- alkani
- valovi
- Alkini
- Butan
Radovednost
Kemik Kekulé je strukturo benzena odkril po sanjah, v katerih je videl strukturo kot kačo, ki pogoltne rep.


