Reakcije substitucije (sinteze) so tiste, ki se pojavijo, ko skupina danega reagenta spremeni položaj s skupino drugega reagenta. Najpogosteje se pojavijo v visoko stabilnih spojinah (tistih z nasičenimi verigami). Pogosto se te sinteze pojavijo s sodelovanjem toplote ali ultravijolične svetlobe v reakcijskem mediju.
Ti alkani so organske spojine, ki so nagnjene k substitucijskim reakcijam, saj imajo le nasičene verige (le preproste vezi med ogljikovimi atomi). Veliko se uporabljajo za sinteze, ki izvirajo iz organskih halogenidov, na primer metilklorid (plin, ki se uporablja kot anestetik).
Najpogostejše substitucijske reakcije z alkani so:
halogeniranje;
nitriranje;
sulfoniranje;
a) halogeniranje
Gre za sintezo, pri kateri molekula alkana reagira z molekulo halogena (Cl2, br2, JAZ2 in F2). Uporaba I2 ni tako izvedljiv, ker spodbuja izjemno počasno reakcijo. Že uporaba F2 ni priporočljivo, ker gre za eksplozivno reakcijo, ki uniči organske snovi.
Za halogeniranje alkanov z Br2 ali Cl2 zgodi se,
prisotnost svetlobe (λ) ali močno ogrevanje. Ne glede na uporabljeni halogen bo končni produkt te substitucijske reakcije vedno a organski halid. Zamenjava bo nato potekala med atomom vodika alkanskega ogljika in atomom halogena, kar bo povzročilo organski halid in kislinski halid (anorganska kislina). Glej primer:
Če ima alkan število ogljikovih atomov večje od dveh, bomo vodik zamenjali s halogenom po naslednjem prednostnem vrstnem redu:
H v terciarnem ogljiku> H v sekundarnem ogljiku> H v primarnem ogljiku
V naslednjem primeru lahko vidimo, da je H sekundarnega ogljika nadomeščen z atomom Br.
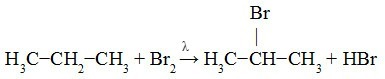
Opazovanje: kadar ima alkan več kot dva ogljika, nastane več kot en organski halid. Količina nastalih halogenidov sledi prednostnemu vrstnemu redu. Oglejte si nekaj primerov:
Bromiranje butana:
V spodnji enačbi opažamo tvorbo 2-bromo-butana (v večji količini, saj je substitucija zaradi izmenjave na sekundarnem ogljiku) in 1-bromo-butana (v manjši meri količina).
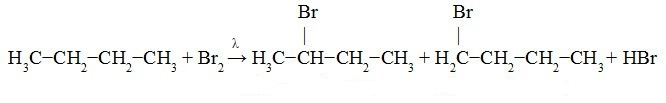
2-bromo-butan 1-bromo-butan
Kloriranje metil propana:

2-kloro-1-kloro-
2-metil-2-metil-
propan propan
Ne ustavi se zdaj... Po oglaševanju je še več;)
b) nitriranje
V tej reakciji dušikova kislina (HNO3) reagira z alkanom tako, da alkanski vodik zamenja z nitro skupino (NO2) kisline, kar ima za posledico a nitro spojina in v molekuli vode. Ker imamo kislino, ni treba uporabljati katalizatorja.
Opazovanje: enaka prednostna pravila, ki se uporabljajo za izmenjavo vodika pri halogeniranju, se uporabljajo pri nitriranju.
Sledi nitriranje pentana:
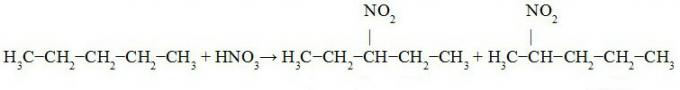
3-nitro-pentan 2-nitro-pentan

1-nitro-pentan
V zgornji enačbi smo opazili tvorbo 3-nitro-pentana (v večji količini, saj je zaradi zamenjave prednost pri zamenjavi izvedemo na terciarnem ogljiku), 2-nitro-pentanu (izmenjava vodika na sekundarnem ogljiku) in 1-nitro-pentanu (v manjših količina).
c) Sulfoniranje
V tej reakciji se žveplova kislina (H2SAMO4) reagira z alkanom tako, da alkanski vodik zamenja za sulfonsko skupino (SO3H) kisline, kar ima za posledico a sulfonska kislina in molekulo vode. Ker imamo kislino, ni treba uporabljati katalizatorja.
Opazovanje: ista prednostna pravila, ki se uporabljajo pri izmenjavi vodika pri halogeniranju, se uporabljajo tudi pri sulfonaciji.
Sledi sulfoniranje pentana:

Penta-3-sulfonska kislina Penta-2-sulfonska kislina
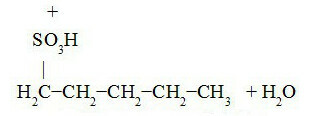
Penta-1-sulfonska kislina
Jaz, Diogo Lopes Dias
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
DNI, Diogo Lopes. "Nadomestne reakcije v alkanih"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-alcanos.htm. Dostopno 28. junija 2021.
Kemija

Alkani, ogljikovodiki, metan, nasičene verige, alifati, parafini, goriva, bencin, mineralni vosek, zemeljsko olje, skrilavci, zemeljski plin, petrokemična industrija.
Nomenklatura alkanov, ogljikovodikova funkcija, valenca ogljika, Mednarodna zveza Ljubljana Čista in uporabna kemija, IUPAC, nasičeni alifatski ogljikovodiki, enojne vezi, spojine Ekološko.
Kemija

Kliknite tukaj in izveste več o substitucijski reakciji, kemičnem postopku, pri katerem uporabljeni reagenti (organski in anorganski) izmenjujejo eno od svojih komponent in tvorijo nove snovi. Med snovmi, ki se najpogosteje uporabljajo kot reagenti, so alkani, benzen in organski halogenidi.