Da boste razumeli pojav ionizacija najprej je treba vedeti, kaj so ioni. Upoštevajte spodnjo razlago:
Vsak atom ima enako število protonov in elektronov; zato je vsak atom električno nevtralen. Poleg tega imajo snovi, ki jih tvorijo skupine atomov, tudi ravnotežje električnega naboja in so električno nevtralne.
Vendar, atom ali skupina atomov lahko izgubi ali pridobi elektrone; ko se to zgodi, izgubijo nevtralnost in postanejo ioni.
Če atom ali skupina atomov izgubi elektrone, bo pozitivno napolnjena in bo imenovan ion kation. Če pa pridobite elektrone, bo naboj negativen, ion pa a anion.
Anorganske snovi so ionske ali imajo sposobnost tvorbe ionov.
Eden od načinov za tvorbo ionov je tako, da se molekulske snovi dajo v vodo, torej tvorijo kovalentne vezi, v katerih se delijo elektroni.
Na primer, če preizkusimo električno prevodnost klorovodikove kisline (HCl) v vodni raztopini (vodikov klorid raztopljena v vodi), bomo videli, da je raztopina elektrolitska, to pomeni, da prevaja električni tok, ker so v tem ioni rešitev.

To pomeni, da je voda delovala kot reaktant in tvorila ione iz klorovodikove kisline. To se zgodi v skladu s spodnjo reakcijo:
Ne ustavi se zdaj... Po oglaševanju je še več;)
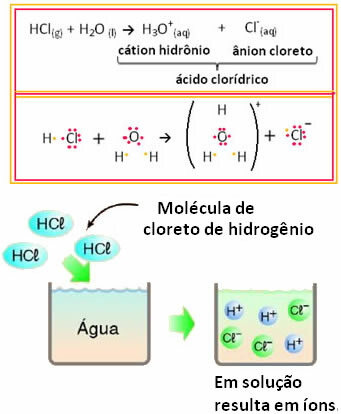
Upoštevajte, da pred dajanjem vodikovega klorida v vodo ni bilo ionov. Njegove molekule pa so reagirale z vodo in tvorile pozitivne H ione3O+ (kationi) in negativi Cl- (anioni). Ker je klor bolj elektronegativen kot vodik, privabi par elektronov iz kovalentne vezi blizu njega in tvori anion. Vodik pa privlači kisik v vodi, ki je bolj elektronegativen kot klor; in med vodikom in kisikom se tvori kovalentna vez, ki povzroči hidronijev kation. Ta pojav tvorbe ionov se imenujeionizacija.
Na podlagi zgornje razlage lahko ionizacijo določimo na naslednji način:

Upoštevajte, da ioni prej niso obstajali, saj bi, če bi obstajali, kot v primeru raztapljanja ionskih spojin, imeli ionsko disocijacijo in ne ionizacijo.
Vse kisline, ki so v stiku z vodo, se ionizirajo. Vendar se vsaka molekularna spojina ne ionizira.Na primer sladkor (C12H22O11) je molekularna, vendar se v vodi ne tvorijo ioni, temveč se samo raztopi, pri čemer nastane neelektrolitska molekularna raztopina, ki ne prevaja elektrike.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Ionizacija"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/ionizacao.htm. Dostopno 28. junija 2021.


