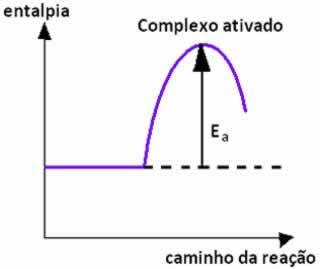
Učinek katalizatorja je v bistvu pospešiti razvoj določene reakcije. To je mogoče, ker katalizator spremeni mehanizem, po katerem poteka reakcija, kar vodi do "alternativne poti", ki zahteva manj aktivacijske energije, da se reakcija začne in doseže aktiviran kompleks.
Obstaja več vrst katalize, med katerimi je ena heterogena kataliza, ki ga lahko definiramo kot tisto, ki se zgodi, ko ima sistem več kot eno fazo, to je, da so reaktanti in produkti v agregatnem stanju, ki se razlikuje od agregatnega stanja katalizatorja.
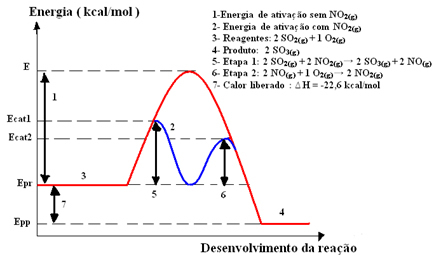
Primer, ki ga lahko omenimo, je vmesna stopnja tvorbe žveplove kisline (H2SAMO4 (aq)). Ta korak je sestavljen iz tvorbe žveplovega trioksida (SO3 (g)) z reakcijo izgorevanja žveplovega dioksida (SO2 (g)):
2 TAKO2 (g) + O2 (g) → 2 OS3 (g)
Ker ta reakcija poteka tako počasi, se za njeno pospešitev uporablja katalizator. Katalizator, ki ga lahko uporabimo v tem primeru, je divanijev pentoksid (V2O5 (S)), kar je solidno. Ker so reaktanti in reakcijski produkti plinasti, bomo imeli heterogen sistem.
Toda kako lahko divanijev pentoksid pospeši reakcijo?
Zgodi se tako, da se molekule kisikovega reagenta adsorbirajo, torej zadržijo na površini divanijevega pentoksida. To povzroči, da vezi molekul tega plina sčasoma oslabijo, kar olajša nastanek kompleksa aktivira in posledično zmanjša aktivacijsko energijo reakcije in poveča njeno hitrost razvoja, to je njeno hitrost.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Oglejte si, kako se to zgodi na spodnjem diagramu:
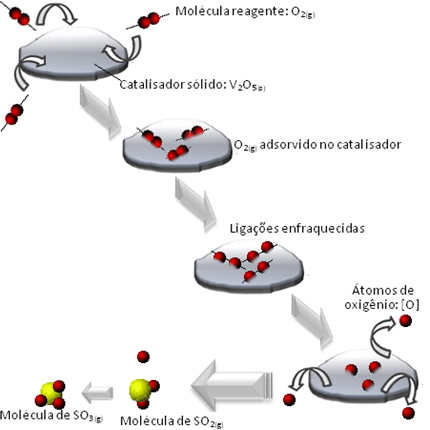
Drugi primeri heterogene katalize so prikazani spodaj. Upoštevajte, da so v obeh primerih reaktanti in produkti v plinastem, vodnem ali tekočem stanju, medtem ko so katalizatorji v trdnem stanju:
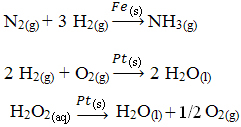
Primer heterogene katalize, ki se pojavlja v našem vsakdanjem življenju, je pretvornik katalitični avto, bolj znan kot katalizatorji. Te naprave proti onesnaževanju so prevlečene s snovmi, ki so katalizatorji običajno zlitina paladija in rodija (za bencinske motorje) ter paladija in molibdena (za bencinske motorje). alkohol).
Znotraj tega katalizatorja pride do kemičnih reakcij, pri katerih se plini iz nepopolnega zgorevanja, ki so za človeka bolj škodljivi, pretvorijo v nestrupene pline. Reaktanti in proizvodi so vsi plini, medtem ko so katalizatorji trdne snovi.
Če želite razumeti več o operacijskem sistemu te opreme, preberite besedilo: "Katalizator”.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Heterogena kataliza"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm. Dostop 27. junija 2021.