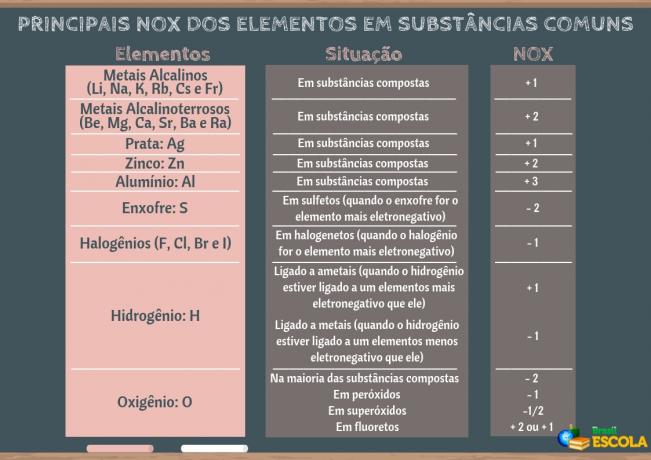
THE Zakon o hitrosti reakcije povezuje hitrost kemične preobrazbe s koncentracijami reagentov v količini snovi (mol / l), ki jo lahko navedemo na naslednji način:

Na primer, upoštevajte naslednjo generično reakcijo:
aA + bB → cC + dD
Recimo, da povečamo koncentracijo reaktantov A in B, kaj se bo zgodilo s hitrostjo reakcije? No, ker se bo količina reaktantnih delcev v istem prostoru povečala, bo prišlo do učinkovitejših trkov med njimi, kar bo povzročilo povečanje hitrosti razvoja reakcije. Kar pomeni, da bo povečala vašo hitrost.
Zato je hitrost reakcije neposredno sorazmerna s koncentracijo reaktantov. Je pa odvisno tudi od temperature. Zato imamo naslednjo matematično enačbo, ki predstavlja zakon reakcijske hitrosti:

Na čem:
v = hitrost reakcije;
k = konstanta, ki je odvisna samo od vrednosti temperature;
α in β = eksperimentalno določeni eksponenti.
Šele ko je reakcija osnovna, torej v enem koraku, so eksponenti popolnoma enaki koeficientom uravnotežene kemijske enačbe: v = k. [THE]The. [B]B
. V drugih primerih pa je treba poskusno določiti primerno jakost, do katere je treba povišati koncentracijo vsakega reagenta.Ne ustavi se zdaj... Po oglaševanju je še več;)
Zakon o hitrosti reakcij se imenuje več, tukaj je nekaj: Zakon o množičnem delovanju, enačba hitrosti, kinetični zakon reakcije in zakon Guldberg-Waage.
Poglejmo primer uporabe tega zakona:
Upoštevajte naslednjo osnovno reakcijo:
2 HCl (g) → H2 (g) + Kl2 (g)
a) Napišite enačbo za hitrost te reakcije;
b) S poskusi smo v spodnji tabeli zabeležili hitrost te reakcije razgradnje vodikovega klorida in koncentracijo tega reagenta pri konstantni temperaturi 25 ° C:
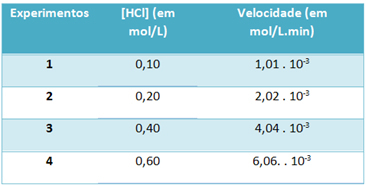
Na podlagi tega določimo značilno konstanto hitrosti te reakcije pri omenjeni temperaturi.
Resolucija:
The) v = k. [HCl]2
b) v = k. [HCl]2
k = __v___
[HCl]2
k = 1,01. 10-3 mol. L-1. min-1
0,01 mol. L-1
k = 1,01. 10-1 min-1
Za rešitev črke "b" lahko uporabite podatke katerega koli od poskusov, da bo dobljena vrednost enaka.
Kaj pa, če reakcija ni osnovna? Kako bo mogoče takšna vprašanja razrešiti v neelementarnih reakcijah? Če želite izvedeti, kako, preberite zakon hitrosti za neelementarne reakcije.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Zakon o hitrosti kemičnih reakcij"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm. Dostop 27. junija 2021.