V besedilu "Naslov ali masni odstotek”Videli smo, kako izračunamo razmerje med maso topljene snovi in maso raztopine za trdne, tekoče in plinaste raztopine. V tem besedilu pa bomo videli, da je možno izračunati tudi titer glede na prostornino za raztopine s tekočimi ali plinastimi komponentami.

Naslov v obsegu lahko izračunamo z izrazom:
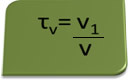
Za primer poglejmo vodno raztopino etilnega alkohola, ki se uporablja kot antiseptik in razkužilo, ki je bila pripravimo z dodajanjem 70 ml čistega alkohola v toliko vode, da dobimo prostornino 100 ml rešitev. Torej imamo:
τ = 70 ml = 0,7
100 ml
Naslov lahko izrazimo tudi v odstotkih, rezultat pa samo pomnožimo s 100%. V tem primeru imamo torej 70% raztopino etilnega alkohola, kar pomeni, da je od vsakih 100 volumskih enot raztopine 70 volumskih enot alkohola.
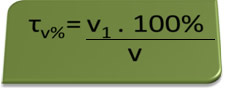
V spodnjem primeru imamo 70% raztopino etilnega alkohola v 250 ml volumna raztopine; kar pomeni, da je po izračunih 175 ml alkohola:
100 ml 70 ml alkohola
250 ml x
x = 70. 250
100
X = 175 ml alkohola

Vendar ne moremo reči, da imamo v tem primeru 75 ml (250-175) vode. Za razliko od masnega titra, pri katerem masi topil lahko dodamo maso topila, da poiščemo maso raztopine, tega glede na volumski titer ni mogoče storiti.

Ne ustavi se zdaj... Po oglaševanju je še več;)
To pomeni, da prostornina raztopine ni enaka vsoti prostornine topila in prostornine topljene snovi (čeprav je pogosto razlika lahko zanemarljiva). To je zato, ker medmolekularne sile, ki obstajajo v teh tekočinah, vplivajo na končni volumen.
V primeru omenjene raztopine, na primer etilnega alkohola, ko na primer zmešamo alkohol z vodo, pride do krčenja celotne prostornine raztopine; to pomeni, da bo končni volumen manjši, kot če bi dodali samo količino alkohola in vode. To je zato, ker molekule alkohola z molekulami vode vzpostavijo vezi ali vodikove vezi in tako zmanjšajo razmike med njimi.
Zato je treba v tem in drugih primerih prostornino raztopine izmeriti eksperimentalno, če v vaji ni predvidena.
Prostorninski odstotek se pogosto uporablja v primeru alkoholnih pijač in komercialnega alkohola, kot je navedeno zgoraj. Oglejte si dve pomembni aplikaciji tega izračuna:
- Alkotest: alkotest meri koncentracijo etilnega alkohola v krvi, v Braziliji pa je prepovedano voziti katero koli vrsto vozila z vsebnostjo alkohola v krvi 0,1% ali več. Oseba s to vsebnostjo alkohola ima za vsak liter krvi 1 ml alkohola, kot kažejo naslednji izračuni:
τv%=V1. 100%
v
0,1 % = V1. 100%
1L
V1 = 0,1% → V1 = 0,001 L = 1 ml
100%

- Vsebnost etanola v bencinu: v Braziliji se bencin regulira z dodatkom etanola. Vsebnost etanola v bencinu pa mora biti največ 24 vol.% Brezvodnega alkohola (ker mora biti bencin brez vode). Čim več etanola dodamo bencinu, tem bolj se barva goriva sveti in njegova gostota narašča.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Naslov zvezka kemične raztopine"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm. Dostopno 28. junija 2021.
Kemija

Kako deluje alkotest, koncentracija alkohola, alkotest, reakcije z etilnim alkoholom, vrste alkotesti, kalijev dikromat, gorivne celice, katalizator, sproščanje elektronov, ocetna kislina, vodik, konce