O izračun atomska masa elementa je matematični vir, ki se uporablja za določanje masne vrednosti, prisotne v periodnem sistemu vsakega od obstoječih kemijskih elementov. Na splošno za izvedbo izračun atomske mase, poznati moramo naslednje spremenljivke kemični element:
Izotopi elementov;
Masno število vsakega izotopa elementa;
Odstotek vsakega izotopa elementa v naravi.
Izračun atomske mase vodika je bil na primer izveden na podlagi naslednjih podatkov:
Predstavlja izotope protiuma (H1), devterij (H2) in tritij (H3);
Mase teh izotopov so 1, 2 oziroma 3;
Odstotek procija v naravi je 98,9%;
Odstotek devterija v naravi je 0,09%;
Odstotek tritija v naravi je 0,01%.
Matematični standard za izračun atomske mase
Za izvedbo izračun atomske mase katerega koli kemičnega elementa moramo uporabiti naslednji matematični vzorec:
1O: množi masno število vsakega izotopa z njegovim odstotkom;
2O: dodaj vse rezultate, najdene v množenju v prvem koraku;
3O: najdeno vsoto razdeli na 100.
M.A. = masno število.odstotek + masno število.odstotek
100
Zemljevid uma: atomska masa
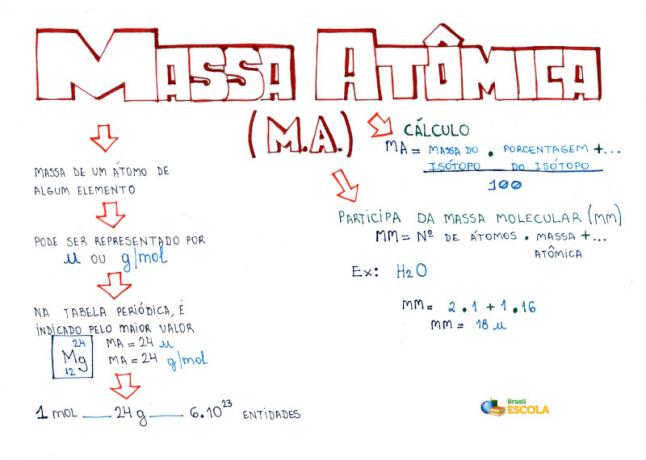
* Če želite prenesti miselni zemljevid v PDF, Klikni tukaj!
Primeri izračuna atomske mase
Example 1. primer: Izračun atomske mase žvepla.
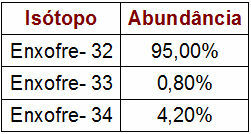
Podatki o odstotkih in masi žveplovih izotopov
Tabela prikazuje masno število in odstotek vsakega žveplovega izotopa v naravi. Za izračun atomske mase preprosto izvedite naslednje korake:
1O Korak: množi masno število vsakega izotopa z vrednostjo njegove številčnosti.
Žveplo - 32 (S.32)
s32 = 32.95
s32 = 3040
Žveplo - 33 (S.33)
s33 = 33.0,8
s33 = 26,4
Žveplo - 34 (S.34)
s34 = 34.4,2
s34 = 142,8
2O Korak: prištejmo vrednosti, ki jih najdemo v množenjih masnega števila in številčnosti izotopa.
Vsota = S32 + S33 + S34
Vsota = 3040 + 26,4 + 142,8
Vsota = 3209,2
3O Korak: atomsko maso izračunamo tako, da vsoto najdenih rezultatov delimo s 100:
M.A. = Vsota
100
M.A. = 3209,2
100
M.A. = 32,092 u
Example 2. primer: Dani kemični element (D) ima tri izotope, katerih masna števila so:
30D 32D 34D
Če vemo, da je atomska masa tega elementa 32,20 u in da je 20% izotopa 32D v naravi, kolikšna je vrednost odstotkov drugih izotopov?
Izjava podaja masna števila, atomsko maso in odstotek enega od izotopov. Za določitev odstotkov drugih izotopov moramo izvesti naslednje korake:
1O Korak: določite odstotek vsakega izotopa.
Izotop - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Izotop - 32 (DS32)
DS32 = 32.20
DS32 = 640
Izotop - 34 (D34)
DS34 = 34.g
DS34 = 34 let
2O Korak: uporabite vse podatke v matematičnem izrazu za izračun atomske mase.
M.A. = masno število.odstotek + masno število.odstotek
100
32,2 = 30x + 640 + 34 let
100
32,2.100 = 30x + 640 + 34 let
100
3220 - 640 = 30x + 34 let
30x + 34y = 2580
x = 2580 - 34 let
30
3O Korak: uporabite zgornji izraz iz naslednjih razlogov:
Odstotek izotopa 1 + Odstotek izotopa 2 + Odstotek izotopa 3 = 100%
x + 20 + y = 100
x + y = 100 - 20
x + y = 80
x = 80 - y
2580 - 34 let = 80-let
30
2580 - 34y = 30. (80-let)
2580- 34 let = 2400 - 30 let
2580 - 2400 = 34 do 30 let
4y = 180
y = 80
4
y = 45%
4O Korak: izračunajte odstotno vrednost x v izrazu, sestavljenem v tretjem koraku.
x + y = 80
x + 45 = 80
x = 80 - 45
x = 35%
Jaz, Diogo Lopes Dias
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm
