Теория гибридизации возникла как дополнение к Теория октетов, сумев объяснить структуру большего числа молекул, включая молекулы, образованные бором (B).
Этот элемент имеет пять электронов в основном состоянии со следующей электронной конфигурацией:
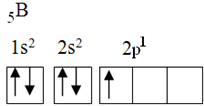
Согласно теории октетов, бор может образовывать только одну ковалентную связь, поскольку у него только одна неполная атомная орбиталь. Однако экспериментально замечено, что этот элемент образует соединения, в которых выполняет более одной связи.
Примером может служить трифторид бора (BF3). Как показано ниже, бор образует три ковалентные связи с фтором, разделяя три пары электронов и имеющий шесть электронов в своей последней оболочке (валентном слое), т. е. исключение из правила октет.
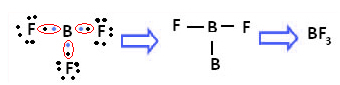
Это объясняется явлением гибридизации, которое происходит с бором. Оказывается, электрон с подуровня 2s поглощает энергию и переходит в возбужденное состояние, в котором он перескакивает на пустую орбиталь подуровня 2p. Таким образом, образуются три неполные орбитали, которые теперь могут образовывать три ковалентные связи:
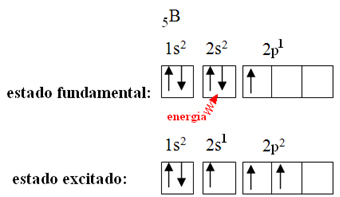
Однако связи, образующиеся в трифториде бора, одинаковы, но если мы посмотрим выше, есть две связи разные, так как один из них будет создан с помощью s-орбитали, а два других - с помощью орбитали типа. введите p. Здесь происходит гибридизация, то есть неполные орбитали сливаются, в результате чего возникает три гибридные орбитали или же гибридизированный, которые идентичны и отличаются от оригиналов:
Не останавливайся сейчас... После рекламы есть еще кое-что;)
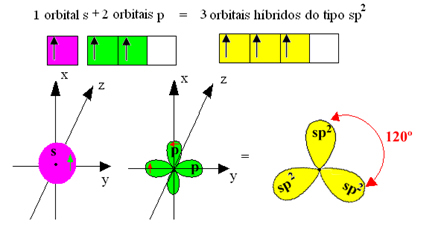
Поскольку эти гибридные орбитали состоят из одной s-орбитали и двух p-орбиталей, такая гибридизация называется sp² гибридизация.
Фтор, который связывается с бором, имеет девять электронов. Его электронное распределение и орбитали показаны ниже:
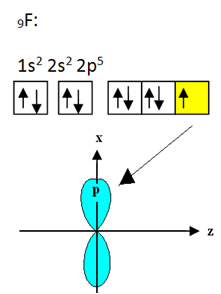
Обратите внимание, что каждый атом фтора может образовывать только одну ковалентную связь и что орбиталь, образующая эту связь, имеет тип p. Итак, посмотрите ниже, как формируются орбитали при создании соединений, образующих BF.3 и посмотрите, насколько ссылки идентичны, например σp-sp2:
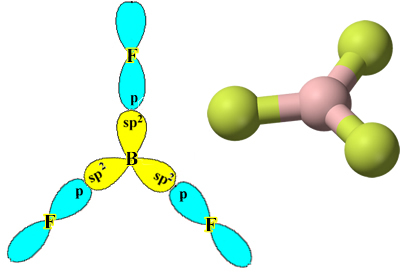
То же самое происходит и с другими элементами, см., Например, текст «Гибридизация бериллия”.
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Гибридизация бора»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm. Доступ 28 июня 2021 г.
