Обычно реакции водный электролиз а также магматический электролиз они проводятся с графитовыми и платиновыми электродами, которые не участвуют в реакции; они проводят только электрический ток. Однако есть некоторые специфические случаи, когда необходимо использовать активные электроды, то есть подвергающиеся восстановлению и окислению.
Основные варианты использования этих электродов, участвующих в окислительно-восстановительном процессе: электролитическая очистка металлов, такие как цинк, кобальт, никель и особенно медь; а также гальваника. Посмотрим, как происходит каждый случай:
• Электролитическая очистка меди: это электролитическое рафинирование меди может обеспечить чистоту около 99,9% и в основном используется для производства медные провода, которые, если они имеют наименьшее количество примесей, могут иметь способность проводить очень электрический ток уменьшилось.
Понаблюдайте, как происходит этот процесс, увидев схему электролитической ванны, собранную ниже:

К водному раствору сульфата меди (CuSo
4 (водн.)), Который проводит электричество, так что анод, представляющий собой нечистую металлическую медь, теряет электроны, то есть подвергается окислению, высвобождая свои катионы (Cu2+), которые нанесены на отрицательную пластину. Это могла быть пластина из инертной платины или, что лучше, пластина из чистой меди. Он составляет катод, который восстанавливается по мере осаждения в нем меди. Таким образом, в электродах происходят следующие полуреакции:Не останавливайся сейчас... После рекламы есть еще кое-что;)
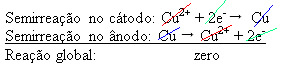
Тот факт, что он дал нулевой результат, указывает на отсутствие химической реакции, а только на перенос меди. На дне контейнера находятся другие нечистые вещества, которые были в меди, такие как золото, серебро, кремнезем (песок) и другие минералы, которые даже можно продать.
• Гальваника: металлическое покрытие наносится на материал, который необходимо защитить от коррозии.
Металл, выбранный для покрытия - это может быть хром (хромирование), никель (никелирование), серебро (серебряное покрытие), золото (золочение) или цинк (гальванизация) - анод, положительный электрод, который подвергается окислению, теряя электроны. Он подвергается окислению вместо материала, который был защищен, потому что его восстановительный потенциал больше.
Отрицательный электрод, то есть катод, который принимает эти электроны и подвергается восстановлению, является самим материалом, на который было нанесено покрытие. Таким образом, он остается защищенным, даже если его поверхность каким-либо образом нарушена.
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Электролиз активными электродами»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm. Доступ 28 июня 2021 г.


