Энтропия это мера степени беспорядка системы, являющаяся мерой недоступности энергии.
Это физическая величина, связанная с Второй закон термодинамики и что оно имеет тенденцию к естественному увеличению во Вселенной.
Определение энтропии
«Беспорядок» следует понимать не как «беспорядок», а как форму организации системы.
Концепция энтропии иногда применяется в других областях знания с этим чувством беспорядка, которое ближе к здравому смыслу.
Например, представьте себе три фляги: одну с маленькими синими шариками, другую с шариками того же типа, но красного цвета, а третью пустую.
Берем пустой горшок и кладем все синие шары снизу и все красные сверху. В этом случае шары разделены и упорядочены по цвету.
При встряхивании кастрюли шары начали перемешиваться таким образом, что в данный момент уже не происходит первоначального разделения.
Даже если мы продолжим трясти горшок, маловероятно, что шары вернутся в ту же первоначальную организацию. То есть упорядоченная система (шары, разделенные цветом) превратилась в неупорядоченную систему (смешанные шары).

Таким образом, естественная тенденция состоит в увеличении беспорядка в системе, что означает увеличение энтропии. Тогда мы можем сказать, что в системах: ΔS> 0, где S - энтропия.
Также поймите, что это такое энтальпия.
Энтропия и термодинамика
Концепцию энтропии начал разрабатывать французский инженер и исследователь Николя Сади Карно.
В своем исследовании преобразования механической энергии в тепловую и наоборот, он обнаружил, что невозможно создать полностью эффективную тепловую машину.
THE Первый закон термодинамики в основном определяет, что «энергия сохраняется». Это означает, что в физических процессах энергия не теряется, а переходит из одного типа в другой.
Например, машина использует энергию для работы, и в этом процессе машина нагревается. То есть механическая энергия превращается в тепловую.
Тепловая энергия не превращается обратно в механическая энергия (если бы это произошло, машина никогда не сломалась бы), поэтому процесс необратим.
Позже лорд Кельвин дополнил исследования Карно о необратимости термодинамических процессов, положив начало основам Второй закон термодинамики.
Рудольф Клаузиус первым использовал термин энтропия в 1865 году. Энтропия будет мерой количества Термальная энергия которые не могут быть превращены в механическую энергию (не могут работать) при определенной температуре.
Клаузиус разработал математическую формулу для изменения энтропии () S), которая используется в настоящее время.
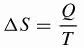
Существование,
ΔS: изменение энтропии (Дж / К)
Q: теплопередача (Дж)
T: температура (K)
Тоже читай:
- Термодинамика
- Цикл Карно
- Энергия
- Типы энергии
- Физические формулы
Решенные упражнения
1) Энем - 2016 г.
До 1824 года считалось, что тепловые двигатели, примерами которых являются паровые двигатели и современные двигатели внутреннего сгорания, могут работать идеально. Сади Карно продемонстрировал невозможность тепловой машины, работающей в циклах между двумя источниками тепла (одним горячим и одним холодным), для достижения 100% эффективности. Такое ограничение возникает из-за того, что эти машины
а) выполнять механические работы.
б) производить повышенную энтропию.
в) использовать адиабатические преобразования.
г) противоречат закону сохранения энергии.
д) работать при той же температуре, что и горячий источник.
Альтернатива: б) производить повышенную энтропию.
2) Энем - 2011 г.
Двигатель может работать только в том случае, если он получает некоторое количество энергии от другой системы. В этом случае энергия, запасенная в топливе, частично высвобождается во время сгорания, чтобы прибор мог работать. Когда двигатель работает, часть энергии, преобразованной или преобразованной при сгорании, не может быть использована для работы. Это означает, что есть утечка энергии в другой форме. Карвалью, А. ИКС. Z.
Теплофизика. Белу-Оризонти: Пакс, 2009 (адаптировано).
Согласно тексту, преобразования энергии, происходящие во время работы двигателя, происходят из-за
а) тепловыделение внутри двигателя невозможно.
б) работа двигателя неконтролируема.
в) полное преобразование тепла в работу невозможно.
г) преобразование тепловой энергии в кинетику невозможно.
д) потенциальное использование энергии топлива неконтролируемо.
Альтернатива: в) полное преобразование тепла в работу невозможно.
Смотри тоже: Упражнения по термодинамике