неорганические соли они образованы ионной ассоциацией по крайней мере одного катиона (образованного любым металлом или аммонием) и аниона (простого или сложного).
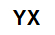
Общая молекулярная формула соли
При добавлении в воду соли диссоциируют, высвобождая по крайней мере один катион, отличный от гидроксония (H+) и анион, отличный от гидроксида (OH-).
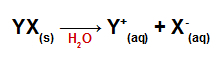
Уравнение диссоциации для любой соли
Классификация солей
Соли, как правило, могут иметь следующие классификации:
простая соль: соль, образованная одним катионом и одним анионом. Примеры: NaCl, CaSO.4, KCN, NH4CO3 и т.п.
Гидрогенизированная соль: он имеет два катиона (один из которых должен быть гидроксонием) и анион. Примеры: NaHCO3, CaHBO3 и т.п.
Гидроксильная соль: он имеет катион и два аниона (один из которых должен быть гидроксидом). Примеры: MgOHCl, Al (OH).2ClO3 и т.п.
Гидратированная соль: представляет молекулы воды, связанные с ее кристаллической структурой. Примеры: CaCl2.2H2О, CuSO4.6H2И т. Д.
Двойная соль: он имеет два катиона (все отличные от гидроксония) и один анион или один катион и два аниона (все отличные от гидроксида). Примеры: Тип
4CN, AgFeBO3 и т.п.Квасцы: представляет собой соль, образованную двумя сульфатами с катионами NOx, равными +1 и +3, плюс 24 молекулы воды. Примеры: Ag2ТОЛЬКО4.Al2(ТОЛЬКО4)3.24H2на2ТОЛЬКО4.Sb2(ТОЛЬКО4)3.24H2О
Правило наименования соли
Название аниона + название де + катиона
→ K3ПЫЛЬ4
Соль имеет фосфат-анион (PO4-3) и катион калия (K+1), отсюда и название - фосфат калия.
→ Дело3
Соль имеет сульфит-анион (SO3-2) и катион кальция (Ca+2), отсюда и название - сульфит кальция.
ПРИМЕЧАНИЕ: Если катион не является серебром, цинком или элементом, принадлежащим к семействам IA, IIA и IIIA, мы должны указать его NOX римской цифрой перед названием катиона.
→ Cu2ТОЛЬКО4
Соль имеет сульфат-анион (SO4-2) и катион кальция (Cu+1), отсюда и название - медный купорос I.
Гидрогенизированная соль: Для этой соли перед названием аниона мы должны написать префикс, относящийся к количеству водорода в формуле. Этот префикс должен быть отделен от слова водород через дефис.
→ NaHCO3
Соль имеет водород, карбонат-анион и катион натрия, поэтому ее название - моногидрокарбонат натрия.
Гидроксильная соль: Для этой соли перед названием аниона мы должны написать префикс, относящийся к количеству гидроксилов в формуле. Этот префикс должен быть отделен от слова гидрокси через дефис.
→ Al (ОН)2ClO3
Соль имеет два гидроксила, хлорат-анион и катион алюминия, поэтому ее название - дигидроксихлорат алюминия.
Гидратированная соль: Для этой соли после названия катиона мы должны написать префикс, относящийся к количеству молекул воды в формуле. Этот префикс должен быть отделен от слова гидратированный через дефис.
→ CaCl2.2H2О
Соль состоит из двух молекул воды: аниона хлорида и катиона кальция, поэтому ее называют дигидратом хлорида кальция.
Двойная соль с двумя катионами: Для этой соли мы должны написать двойное слово в скобках после названия аниона, а затем название наиболее электроположительного катиона и другого катиона.
→ AgFeBO3
Эта соль содержит серебро (более электроположительный катион) и катион железа II, помимо борат-аниона. Его название - борат (двойник) серебра и железа II.
-
Двойная соль с двумя анионами:
Название наиболее электроотрицательного аниона + дефис + название наименее электроотрицательного аниона + название де + катиона
→ Тип4CN
Эта соль содержит катион титана IV, помимо фосфата (более электроотрицательный анион) и цианид-аниона. Его название - цианид-фосфат титана IV.
Квасцы: Для этой соли мы игнорируем общее правило. Просто напишите термин квасцы, за которым следует название катиона заряда +3 и название катиона заряда +1, соответственно, разделенные соединением e.
→ В2ТОЛЬКО4.Sb2(ТОЛЬКО4)3.24H2О
Квасцы имеют катион сурьмы +3 и катион натрия +1, поэтому ее называют квасцами сурьмы III и натрием.
Физические характеристики солей
Они твердые при комнатной температуре;
У них высокие температуры плавления и кипения;
Они образованы ионными связями;
Они проводят электрический ток в жидком состоянии (после плавления) или при растворении в воде;
Вообще говоря, они растворимы в воде, но есть соли, которые считаются практически нерастворимыми.
Химические свойства солей
Соли - это соединения, которые обладают способностью химически реагировать (при условии, что они не содержат тот же катион или тот же анион, что и другое вещество) с несколькими группами веществ, а именно:
В реакции двойного обмена с кислотой: они образуют новую соль и новую кислоту.
В реакции двойного обмена с основанием: они образуют новую соль и новое основание.
В реакция двойного обмена с другой солью: образуют две новые соли.
Некоторые соли обладают способностью страдать разложение при нагревании образует два или более новых вещества. Если нагреть бикарбонат натрия (NaHCO3), например, он разложится, образуя карбонат натрия (Na2CO3), вода (H2O) и диоксид углерода (CO2).
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm
