двойная соль это название, данное одной из классификаций, неорганические соли можно получить. Другие классификации: простые, квасцы, гидроксилированный, гидрогенизированный и гидратирован. Чтобы характеризоваться как двойная соль, неорганическая соль должна иметь одну из комбинаций, описанных ниже:
Катион (Y) и любые два аниона (X и W) представлены следующей формулой:
YXW
Анион (X) и любые два катиона (Y и Z) и представлены следующей формулой:
YZX
Примечание: Эти соли образуются, когда реакция нейтрализации выполняется между двумя базы разные и один кислота, или между двумя разными кислотами и основанием.
Правило именования двойной соли
Чтобы назвать двойная соль, необходимо, во-первых, узнать его состав, потому что для каждого типа двойной соли существует определенное правило именования, как показано ниже:
а) Правило номенклатуры двойной соли с двумя катионами
Когда один двойная соль имеет два катиона, мы должны использовать следующее правило:

Правило номенклатуры, используемое для двойных солей с двумя катионами
Ниже приведены два примера применения этого правила именования:
1-й пример: Линия4s
Эта соль состоит из:
Анион: сульфид (S-2);
Более электроположительный катион: литий (Li+1);
Менее электроположительный катион: аммоний (NH4+1).
Отсюда его название - сульфид лития (двойной) аммония.
2-й пример: RbCaBO3
Эта соль состоит из:
Анион: борат (BO3-3);
Более электроположительный катион: рубидий (Rb+1);
Менее электроположительный катион: кальций (Ca+2).
Таким образом, его название - борат (двойник) рубидия и кальция.
б) Правило номенклатуры двойной соли с двумя анионами
Когда один двойная соль имеет два аниона, мы должны использовать следующее правило:
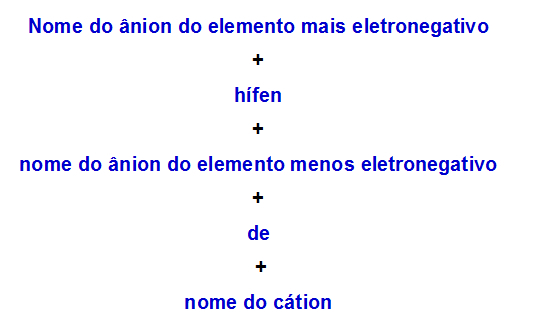
Правило номенклатуры, используемое для двойных солей с двумя анионами
Вот два примера применения этого правила:
1-й пример: MgFI
Эта соль состоит из:
Катион: магний (Mg+2);
Наиболее электроотрицательный анион: фторид (F-1);
Менее электроотрицательный анион: йодид (I-1).
Поэтому его название - фторид-йодид магния.
2-й пример: ZnNO2br
Эта соль состоит из:
Катион: цинк (Zn+2);
Более электроотрицательный анион: нитрит (NO2-1);
Менее электроотрицательный анион: бромид (Br-1).
Отсюда его название - нитрит-бромид цинка.
Составление формулы двойной соли из ее номенклатуры
а) Для двойной соли с двумя катионами
Построение формулы двойная соль это зависит от знания его названия, которое, как и все соли, стандартизировано, то есть сначала катион, а затем анион. Поскольку двойная соль может иметь два катиона, их порядок и расположение в формуле соответствуют заданному имени.
1-й пример: пирофосфат никеля бария II
Эта соль содержит фосфат (P2O7), барий (Ba+2) и никель II (Ni+2), катионы, записанные в такой последовательности. Таким образом, его формула - BaNiP2O7.
2-й пример: фосфат меди II и золото I
Эта соль содержит фосфат (PO4-3), медь II (Cu+2) и золото I (Au+1), катионы, записанные в такой последовательности. Следовательно, его формула - CuAuPO4.
б) Для двойной соли с двумя анионами
В случае двойная соль с двумя анионами мы также следим, помещая анионы в формулу, в том порядке, в котором они появляются в данном имени.
1-й пример: сульфат-иодид никеля III
Эта соль имеет сульфат-анионы (SO4-2) и йодид (I-1), записанные в этой последовательности, и катион никеля III (Ni+3). Итак, его формула - NiSO4Я.
2-й пример: цианид фосфат свинца IV
Эта соль содержит фосфат-анионы (PO4-3) и цианид (CN-1), записанный в этой последовательности, и катион свинца IV (Pb+4). Таким образом, его формула PbPO4CN.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm
