К семейства периодических таблиц являются вертикальными последовательностями таблицы и собирают химические элементы со схожими химическими свойствами. Такое сходство связано с наличием равного количества валентных электронов у элементов, сгруппированных в одном семействе. Семьи содержат репрезентативные элементы в группах 1 и 2, с 13 по 18 и переходные элементы в группах с 1 по 12.
Читайте также:Трансурановые элементы - искусственные химические элементы, которые идут после урана в Периодической таблице.
Темы этой статьи
- 1 - Сводка семейств периодической таблицы
- 2 - Организация семейств периодической таблицы
-
3 - Номенклатура семейств периодической таблицы
- → Репрезентативные элементы Периодической таблицы
- → Переходные элементы периодической таблицы
- 4 - Химические элементы семейств периодической таблицы
-
5 - Основные характеристики семейств периодической таблицы
- → Группа 1 или семейство щелочных металлов
- → Группа 2 или семейство щелочноземельных металлов
- → Группы с 3 по 12 или семейство переходных металлов
- → Группа 13 или семейство бора
- → Группа 14 или семейство углерода
- → Группа 15 или семейство азота
- → Группа 16 или кислородное семейство (халькогены)
- → Группа 17 или семейство галогенов
- → Группа 18 или семейство благородных газов
-
6 - Периодическая таблица и электронное распространение
- → Электронное распределение репрезентативных элементов
- → Электронное распределение переходных элементов
- 7 - Решенные упражнения на семейства периодической таблицы
Краткое изложение семейств периодической таблицы
Семейства соответствуют вертикальным линиям Периодическая таблица.
Также известные как группы, семейства в Периодической таблице пронумерованы от 1 до 18.
Химические элементы одного семейства имеют сходные химические свойства.
Привычность набора элементов объясняется наличием равного числа валентных электронов.
Репрезентативные элементы разделены на группы 1, 2, 13, 14, 15, 16, 17 и 18. Каждое из этих семейств имеет определенные имена.
Переходные элементы образуют единое семейство, которое делится на группы 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12.
Не останавливайся сейчас... После рекламы будет больше ;)
Организация семейств периодической таблицы
Семьи в периодической таблице являются вертикальными последовательностями таблицы, то есть столбцы. Также известные как группы, семейства периодической таблицы пронумерованы от 1 до 18 слева направо.
Химические элементы, находящиеся в одном столбце, считаются принадлежащими к одному семейству., из-за сходства между их химическими свойствами, что связано с тем, что они имеют одинаковое количество электроны в валентной оболочки. Например, все химические элементы семейства 18 имеют восемь электронов на валентной оболочке (полная оболочка) и редко участвуют в химические связи.
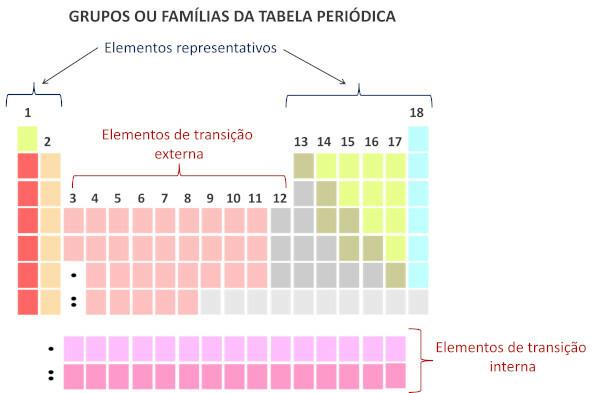
По современной системе Международный союз теоретической и прикладной химии (Юпак), каждая группа или семейство обозначается числом от 1 до 18, начиная слева направо в периодической таблице.
Важно подчеркнуть, что старая система ИЮПАК использовала буквенно-цифровую систему с буквами А и В для обозначения репрезентативных и переходных элементов соответственно. В настоящее время этот тип номенклатуры больше не используется.
Номенклатура семейств периодической таблицы
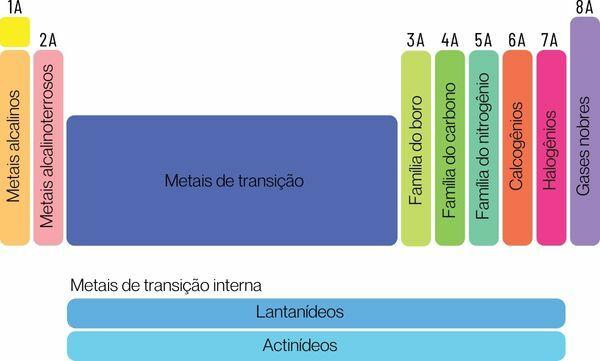
Химические элементы можно разделить на два больших семейства: репрезентативные элементы и переходные элементы.
→ Репрезентативные элементы Периодической таблицы
Репрезентативные элементы разделены на группы 1, 2, 13, 14, 15, 16, 17 и 18. Каждая из этих групп имеет определенное название, под которым она также может быть известна. Смотреть:
Группа 1: семья металлы щелочной.
Группа 2: семья щелочноземельные металлы.
Группа 13: семейство борных или земляных металлов.
Группа 14: семейство углерода.
Группа 15: Семейство азота или пникогенов.
Группа 16: кислородное или халькогеновое семейство.
Группа 17: семья галогены.
Группа 18: семья благородные газы.
→ Переходные элементы периодической таблицы
Ты переходные элементыобразуют единую семью, разделенную на группы 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12.. Ряды лантанидов и актиноидов также входят в состав переходных элементов.
Переходные элементы все металлические и имеют схожие химические свойства, даже имея разные электроны на валентной оболочке и, следовательно, образовывали бы единое и большое семейство переходных металлов.
Химические элементы из семейств периодической таблицы
Каждое семейство или группа состоит из набора химических элементов. См. описание химических элементов, входящих в каждое семейство:
Группа 1:литий, натрий, калий, рубидий, цезий, франций.
Группа 2:бериллий, магний, кальций, стронций, барий, радио.
Группа 3:скандий, иттрий, лантанидный ряд и актинидный ряд.
Группа 4: титан, цирконийО, гафний Это резерфордий.
Группа 5:ванадий, ниобий, тантал Это дубний.
Группа 6:хром, молибден, вольфрам Это сиборгиум.
Группа 7:марганец, технеций, рений Это борио.
Группа 8: железо, рутений, осмий Это гассиум.
Группа 9:кобальт, родий, иридий и мейтнерий.
Группа 10:никельпалладий, платина и дармштадтио.
Группа 11: медь, серебро, золото и рентгений.
Группа 12:цинк, кадмий, Меркурий и Коперник.
Группа 13: бор, алюминий, галлий, индий и таллий.
Группа 14: углерод, кремний, германий, банка, вести и флеровий.
Группа 15:азот, люминофор, мышьяк, сурьма Это висмут.
Группа 16:кислород, сера, селен, теллур, полоний и ливерморий.
Группа 17: фтор, хлорбром, йод и астатин.
Группа 18:гелий, неон, аргон, криптон, ксенон Это радон.
Важный: химический элемент водород является частным случаем, потому что, несмотря на то, что он расположен рядом с группой 1, он не является частью семейства щелочных металлов, поскольку не обладает аналогичными химическими свойствами.
Узнать больше: Какие радиоактивные элементы входят в периодическую таблицу?
Основные характеристики семейств периодической таблицы
Это металлические твердые тела, блестящие и гладкие.
Они обладают высокой теплопроводностью и высокой Электропроводность.
иметь температуры относительно низкоплавкий.
Они очень реагируют с вода.
Склонность к образованию одновалентных катионов (заряд +1).
Это металлические твердые вещества, блестящие и более твердые по сравнению с щелочными металлами.
Они легко окисляются.
Они обладают высокой теплопроводностью и высокой электропроводностью.
Они имеют несколько более высокую температуру плавления по сравнению с щелочными металлами.
Они реагируют с водой.
Склонность к образованию двухвалентных катионов (заряд +2).
Это самое большое семейство в периодической таблице.
Твердые, блестящие металлические твердые частицы.
Они обладают высокой теплопроводностью и высокой электропроводностью.
Плотный.
Высокая температура плавления.
могут представлять разные степени окисления.
→ Группа 13 или семейство бора
Они обладают промежуточными свойствами между свойствами металлов и не металлы.
Они тверды в условиях окружающей среды.
Склонность к образованию трехвалентных катионов (заряд +3).
→ Группа 14 или семейство углерода
Они обладают промежуточными свойствами между свойствами металлов и неметаллов.
Они тверды в условиях окружающей среды.
Тенденция к образованию четырех связей.
Они тверды в условиях окружающей среды.
Углерод и кремний могут образовывать цепные связи.
→ Группа 15 или семейство азота
Они обладают промежуточными свойствами между свойствами металлов и неметаллов.
Твердые вещества в условиях окружающей среды, за исключением азота, который является газом.
Азот и фосфор являются основными элементами живых организмов.
Мышьяк очень токсичен.
→ Группа 16 или кислородное семейство (халькогены)
У них разные свойства, меняющиеся от неметаллических к металлическим элементам по мере продвижения по семейству.
Твердые вещества в условиях окружающей среды, за исключением кислорода, который является газом.
Склонность к образованию двухвалентных анионов (заряд -2).
→ Группа 17 или семейство галогенов
Они неметаллы.
Довольно реактивный.
Плохие тепловые и электрические проводники.
В условиях окружающей среды фтор и хлор существуют в виде газы, бром жидкий, а йод твердый.
Склонность к образованию одновалентных анионов (заряд -1).
→ Группа 18 или семейство благородных газов
Они неметаллы.
Очень мало реактивны, поэтому их можно назвать инертными газами.
Они существуют в виде газов.
Они не имеют склонности к образованию ионы.
Периодическая таблица и электронное распространение
Химические элементы, принадлежащие к одному и тому же семейству или группе, имеют сходные химические свойства, потому что они одинаковое количество электронов на валентной оболочке.
Количество электронов на валентной оболочке имеет значение, так как оно определяет склонность к образованию катионов или анионы, тип образующейся химической связи, энергия, связанная с химическими реакциями, среди прочего характеристики. Чтобы найти число валентных электронов, необходимо знать атомный номер элемента и выполнить свой электронная дистрибуция.
→ Электронное распределение репрезентативных элементов
Репрезентативные элементы имеют наиболее энергичные электроны на подуровнях с Это п электронного слоя (n). В следующей таблице собраны электронные конфигурации, связанные с каждым семейством репрезентативных элементов. термин н варьируется от 1 до 7 и представляет собой энергетический уровень, занимаемый валентными электронами, эквивалентный периоду (горизонтальная линия) периодической таблицы, в которой находится элемент.
Электронное распределение репрезентативных элементов | ||
семья или группа |
Электронная дистрибуция |
Пример |
1 |
нас1 |
Ли (Z=3): 1с2 2 с1 |
2 |
нас2 |
Быть (Z=4): 1с2 2 с2 |
13 |
нас2 нп1 |
Б (Z=5): 1 с2 2 с22р1 |
14 |
нас2 нп2 |
С (Z=6): 1 с2 2 с22р2 |
15 |
нас2 нп3 |
N (Z=7): 1 с2 2 с22р3 |
16 |
нас2 нп4 |
O (Z=8): 1 с2 2 с22р4 |
17 |
нас2 нп5 |
F (Z=9): 1 с2 2 с22р5 |
18 |
нас2 нп6 |
Ne (Z=10): 1 с2 2 с22р6 |
→ Электронное распределение переходных элементов
Переходные элементы распределены между группами 3 и 12 и иметь подуровни д Это ф заняты валентными электронами:
Внешние переходные элементы: удерживать валентные электроны на подуровне д, сохраняя электронную конфигурацию равной нас2 (н-1)д(от 1 до 8). Например, элемент никель (Z = 28) относится к группе 10, и его конфигурация 1s2 2 с2 2р6 3 с2 3р6 4 с2 3д8.
Внутренние переходные элементы: они входят в группу 3, но являются «внутренними» по отношению к Периодической таблице, расширяясь ниже ее, в периоды 6 (лантаноиды) и 7 (актиниды). Эти элементы имеют валентные электроны, занимающие подоболочку ф и общая электронная конфигурация нас2 (п-2)ф(от 1 до 13). Например, элемент лантан (Z = 57) является первым элементом в ряду лантаноидов, и его электронная конфигурация равна 1s.2 2 с2 2р6 3 с2 3р6 4 с2 3д10 4р6 5 с2 4д10 5р6 6 с2 4f1.
Знай также:Каково происхождение Периодической таблицы?
Решенные упражнения на семейства периодической таблицы
Вопрос 1
(UFC — адаптировано) Относительно современной периодической классификации элементов отметьте верное утверждение:
А) В периодической таблице семействам или группам соответствуют горизонтальные линии.
Б) Элементы одного семейства имеют очень разные химические свойства.
в) Элементы семейства обычно имеют одинаковое число электронов на последней оболочке.
Г) В периоде элементы имеют сходные химические свойства.
E) Репрезентативные элементы распределены по группам с 3 по 12.
Разрешение:
Альтернатива С
Пункт А неверен: семейства или группы являются столбцами (вертикальными линиями) периодической таблицы.
Пункты B и D неверны: в одном семействе элементы имеют сходные химические свойства. В периоды элементы имеют одинаковую электронную оболочку, занятую валентными электронами.
Правильный пункт C: в семье элементы имеют одинаковое количество электронов на последней оболочке.
Пункт E неверен: репрезентативными элементами являются группы 1, 2, 13, 14, 15, 16, 17 и 18. Переходные элементы распределены по группам с 3 по 12.
вопрос 2
(EAM) Элементы A, B и C имеют следующие электронные конфигурации в своих валентных оболочках:
А: 3с1
Б: 4с2 4р4
С: 3 с2
На основании этой информации выберите правильный вариант.
А) Элемент А – щелочной металл.
Б) Элемент Б представляет собой галоген.
C) Элемент C является халькогеном.
Г) Элементы А и В относятся к третьему периоду Периодической таблицы.
E) Три элемента принадлежат к одной и той же группе Периодической таблицы.
Разрешение:
Альтернатива А
Пункт А правильный: элемент А имеет электронное распределение, содержащее только один валентный электрон, поэтому он принадлежит к группе 1 Периодической таблицы.
Неверный элемент B: элемент B имеет 4s-электронную конфигурацию.2 4р4, что указывает на то, что на последней оболочке 6 электронов и что этот элемент принадлежит к группе 16 (халькогены).
Неверный пункт C: элемент C имеет электронную конфигурацию с 2 электронами в последней оболочке, поэтому он является элементом группы 2 в таблице.
Неверный пункт D: элемент A относится к третьему периоду (n = 3), а элемент B принадлежит к четвертому периоду (n = 4).
Неверный пункт E: три элемента имеют разное количество электронов в последней оболочке, поэтому они не могут быть частью одного и того же семейства.
Ана Луиза Лоренцен Лима
Учитель химии
Нажмите здесь, узнайте, что такое валентный слой, и узнайте, как его можно идентифицировать.
Узнайте, как осуществляется электронное распространение, и посмотрите примеры.
Узнайте об особенностях внутренних переходных элементов (актиноидов и лантаноидов), которые занимают шестой и седьмой периоды группы 3 Периодической таблицы.
Знать существующие химические элементы, понимать, что они из себя представляют и как их представлять.
Благородные газы — единственные элементы, встречающиеся в природе в изолированном виде. Узнайте больше о них здесь, в этой статье!
Узнайте о галогенах, их свойствах, характеристиках и их основном использовании в повседневной жизни.
Узнайте больше о щелочноземельных металлах, зная характеристики, свойства и области применения.
Поймите, что такое атомный номер, и узнайте, какие характеристики атома можно определить по нему.
Узнайте здесь, что такое периодическая таблица, и посмотрите интерактивную модель, чтобы вы знали все химические элементы, из которых она состоит.