PH соответствует водородному потенциалу раствора. Он определяется концентрацией ионов водорода (H+) и служит для измерения степени кислотности, нейтральности или щелочности данного раствора.
Помимо pH, существует еще одна величина, которая определяет кислотность и основность водной системы: pOH (гидроксилионный потенциал). Эта шкала выполняет ту же функцию, что и pH, но используется реже.
шкала pH
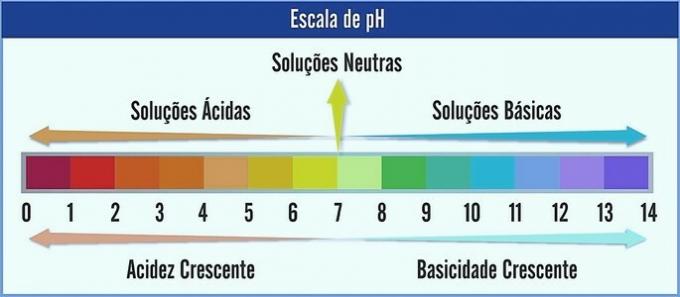
Значение pH представлено по шкале от 0 до 14. Он измеряет кислотность и основность раствора.
Следовательно, pH 7 соответствует нейтральному раствору (например, чистой воде). Те, что до него, считаются кислыми растворами (кислый pH), а те, что после 7 - основными (щелочные pH).
После этого наблюдения кислотный характер усиливается справа налево. Основной персонаж слева направо. Учтите, что чем ниже значение pH, тем более кислым будет раствор.
Узнайте больше на:
- Буферный раствор
- Титрование
- Реакция нейтрализации
Примеры
Кислотные растворы
| Решение | pH |
|---|---|
| Желудочный сок | 2,0 |
| Лимонный сок | 2,2 |
| Уксус | 3,0 |
| Кофе | 5,0 |
| Коровье молоко | 6,4 |
Базовые решения
| Решение | pH |
|---|---|
| человеческая кровь | 7,35 |
| Морская вода | 7,4 |
| Бикарбонат натрия | 8,4 |
| Молоко магнезии | 10,5 |
| Отбеливать | 12,5 |
Как рассчитать pH?
В 1909 году датский химик Сорен Соренсен (1868-1939) предположил, что кислотность растворов, измеряемая по концентрации ионов H+, его значения были преобразованы с использованием логарифмов для облегчения понимания.
При температуре 25 ° C ионное произведение воды равно 10–14 моль2/ Л2.
Применяя одеколон в выражении, мы должны:
С помощью этого выражения мы можем получить соответствующее значение от одной шкалы к другой путем вычитания.
Как измерить pH?
Контроль pH важен не только в научных целях, но и в повседневной жизни.
Необходимо проверить pH бассейна, а также pH аквариума и даже pH почвы, чтобы учесть определенные типы культур.
Ниже приведены основные способы измерения pH.
кислотно-щелочной индикатор
Так называемые кислотно-щелочные индикаторы используются для измерения pH раствора. Это вещества, которые меняют цвет, указывая на характер раствора. Наиболее часто используемые индикаторы: лакмус и фенолфталеин.

Шагомер
Помимо индикаторов, pH раствора можно измерить с помощью прибора, называемого пигометром. Это электронное устройство измеряет электрическую проводимость раствора и преобразует ее в шкалу значений pH.

Упражнения для вступительных экзаменов с обратной связью
1. (Enem / 2014) Исследователь понимает, что этикетка на одном из стаканов, в котором он хранит концентрат пищеварительных ферментов, неразборчива. Он не знает, какой фермент содержит стакан, но подозревает, что это желудочная протеаза, которая работает в желудке, переваривая белок.
Зная, что пищеварение в желудке кислое, а кишечник - основной, он собирает пять пробирок с едой. разные, добавьте концентрат фермента в растворы с определенным pH и подождите, чтобы увидеть, действует ли фермент в каких-либо их.
Пробирка, в которой должен действовать фермент, чтобы показать, что гипотеза исследователя верна, содержит:
а) картофельный кубик в растворе с pH = 9
б) кусок мяса в растворе с pH = 5
в) вареный яичный белок в растворе с pH = 9
г) порция лапши в растворе с pH = 5
д) масляный шар в растворе с pH = 9
Правильная альтернатива: б) кусок мяса в растворе с pH = 5.
Протеаза - это фермент, который переваривает белки, и, поскольку он желудочный, он действует в желудке с кислым pH.
Анализируя альтернативы, мы должны:
а) НЕПРАВИЛЬНО. Картофель богат углеводами, а уровень pH концентрата является основным.
б) ПРАВИЛЬНО. Мясо содержит белки и ферменты, которые могут действовать на него, а pH концентрата кислый, как в желудке.
в) НЕПРАВИЛЬНО. PH концентрата - основной.
г) НЕПРАВИЛЬНО. Паста богата углеводами.
д) НЕПРАВИЛЬНО. PH концентрата - основной.
2. (Udesc / 2009) «Кислотный дождь» - это термин, который относится к дождевым осадкам из атмосферы с большим, чем обычно, количеством азотной и серной кислот.
Предшественники кислотных дождей происходят как от природных источников, таких как вулканы и гниющая растительность, так и от процессов. промышленные выбросы, в основном диоксид серы и оксиды азота от сжигания топлива окаменелости.
Считается нормальным pH дождевой воды 5,5 (из-за присутствия углекислоты в результате солюбилизации диоксида углерода). Химик, наблюдающий за высокоразвитым промышленным регионом, отметил, что pH дождевой воды составляет 4,5.
Учитывая, что кислотность связана с концентрацией H3О+, правильно сказать, что вода с pH 4,5 была:
а) в два раза больше обычного.
б) в два раза более кислой, чем обычно.
в) в десять раз более простой, чем обычно.
г) в десять раз более кислый, чем обычно.
д) в сто раз более кислый, чем обычно.
Правильная альтернатива: г) в десять раз более кислый, чем обычно.
Согласно выражениям pH = - log [H+] и [H+] = 10-pH, Мы должны:
pH = 5,5
[ЧАС+] = 10-5,5
pH = 4,5
[ЧАС+] = 10-4,5
Разница между значениями: 10- 5,5 - ( - 4,5) = 10 -1
Поскольку шкала pH представляет собой логарифмическую шкалу, изменение одной единицы дает в 10 раз более кислый раствор.
3. (UFMG / 2009) Рассмотрим смешанное количество воды и лимонного сока, содержащееся в стакане. Просмотрите эти три утверждения относительно этой системы:
Я. Система кислая.
II. Системный pH больше 7.
III. В системе концентрация ионов H+ больше, чем ОН–.
На основании этого анализа ПРАВИЛЬНО заявить, что:
а) верны только утверждения I и II.
б) верны только утверждения I и III.
в) верны только утверждения II и III.
г) все три утверждения верны.
Правильная альтернатива: б) верны только утверждения I и III.
Я. ВЕРНЫЙ Лимон содержит лимонную кислоту, которая в растворе выделяет ионы H.+ и поэтому система кислая.
II. НЕПРАВИЛЬНЫЙ. Значение pH меньше 7, что характеризует кислую систему: чем ближе pH раствора к 0, тем он более кислый.
III. ВЕРНЫЙ Кислый pH является результатом высокой концентрации ионов H+ в растворе, так как pH = - log [H+].
Для получения дополнительных вопросов с прокомментированным разрешением обязательно проверьте:Упражнения на pH и pOH.