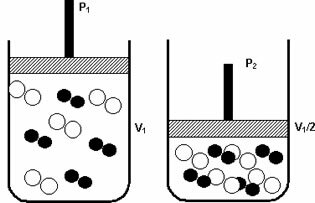
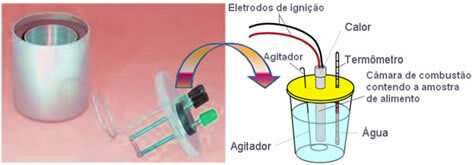
Эндотермические и экзотермические реакции количества, которые измеряют количество тепла (энергии), поглощаемого и выделяемого во время химических реакций. Их изучает термохимия.
В чем разница между ними?
эндотермическая реакция тот, в котором происходит поглощение энергии. В этом процессе производится и независимо поддерживается энергия.
Птицы и млекопитающие обладают способностью поддерживать стабильную температуру тела. По этой причине их называют эндотермическими животными, в народе «теплокровными животными».
Экзотермическая реакция тот, в котором происходит выделение энергии. В этом процессе производство энергии сохраняется только за счет непрерывной подачи энергии.
Изменение физических состояний в таком порядке: газ, жидкость и твердое тело - это пример экзотермической реакции. Каждый из них происходит при высвобождении энергии, то есть при меньшем количестве тепла.
Обратите внимание, что когда мы меняем этот порядок (твердое тело, жидкость и газ), вырабатывается энергия (больше тепла). В этом случае реакция эндотермическая.
Примеры на каждый день
Жир действует как топливо в нашем теле. Тот, что не сгорел, поглощается им. Поскольку это процесс абсорбции, это пример эндотермической реакции.
Ставя сковороду на огонь для приготовления пищи, мы, в свою очередь, сталкиваемся с экзотермическим процессом. Это потому, что выделяемое тепло преобразует эту пищу, чтобы ее можно было употреблять в пищу.
А что такое энтальпия?
энтальпия это энергия, которая присутствует во всех веществах и изменяется в результате эндотермических и экзотермических реакций.
Поскольку вычислить энтальпию невозможно, был произведен расчет ее изменения.
Таким образом, сравнивая стандартную энтальпию (температура 25º C при атмосферном давлении 1 атм), можно было бы вычислить изменение энтальпии.
Согласно Закон Гесса, конечная энтальпия за вычетом начальной энтальпии (ΔH = Hж - Hя) приводит к этим данным.
Если эндотермическая реакция поглощает энергию, это означает, что энтальпия (конечного) реагента ниже, чем энтальпия (исходного) продукта. Следовательно, изменение энтальпии положительное (ΔH> 0).
В свою очередь, если экзотермическая реакция высвобождает энергию, это означает, что энтальпия (энергия) реагента больше, чем у продукта. Следовательно, изменение энтальпии отрицательное (ΔH
Читайте тоже:
- Химические реакции
- Химический баланс
- Горение