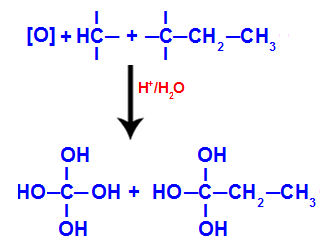
Алкены или алкены - это углеводороды, которые имеют двойную связь в своей углеродной цепи.
Общая формула алкенов: CнетЧАС2n.
Большинство алкенов производится в лаборатории, а некоторые встречаются в природе.
Функции
Основные характеристики алкенов:
- бесцветный
- Не растворим в воде
- Растворим в спирте и эфире
- Они более реакционноспособны, чем алканы.
- Температуры плавления и кипения выше, чем у алканов с таким же числом атомов углерода.
- Самый простой алкен - этилен или этилен.
Также знаете о:
- алканы
- Алкины
- алкадиен
Номенклатура
Алкены получают ту же номенклатуру, что и другие углеводороды.
ПРЕФИКС + ИНФИКС + СУФФИКС
Префикс указывает количество атомов углерода в основной цепи.
Инфикс дается термином «en», который представляет двойную связь. Суффикс обозначается буквой «о», обозначающей углеводородное соединение.
Таким образом, алкены называются суффиксом –Eno, что указывает на двойную связь.
Также необходимо указать положение двойной связи. Это число стоит перед названием алкена и указывает атом углерода, с которого начинается связь.
Углеродная цепь начинает нумероваться от ближайшего конца двойной связи.
Примеры
Этен или этилен: CH2 = CH2
Пропилен или пропилен: CH2 = CH - CH3, эквивалентная формула которой записывается следующим образом: CH3 - CH = CH2
1-бутен: CH2 = CH - CH2 - CH3
2-бутен: CH3 - CH = CH - CH3
Алкены также часто изомерия:
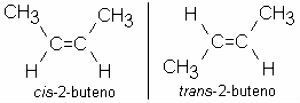
разветвленные алкены
Алкены также могут быть разветвленными. В этом случае основная цепь является самой длинной и имеет двойную связь.
Пример:
5-метил-2-гексан
Узнать больше о Номенклатура углеводородов.
Дополните свое исследование Углеводороды. Читайте тоже:
- Бензол
- Бутан
- Цикланы
- Нефть
- Органические соединения
- Ароматические углеводороды
- Упражнения по углеводородам