О стиральный порошок это чистящее средство, которое является частью повседневной жизни значительной части населения, поскольку оно используется для облегчения стирки одежды людей. Это продукт, который заменил кусковое мыло, поскольку в процессе стирки люди имели привычку натирать им одежду.

Кусковое мыло по-прежнему широко используется при мытье посуды, например
Порошковое мыло было впервые произведено в 1946 году после нескольких попыток упростить использование кускового мыла. Одна из попыток заключалась в производстве мыла в виде хлопьев или гранул. Однако эти попытки не увенчались успехом, потому что мыло взаимодействует с ионами, присутствующими в жесткой воде, в основном ухудшая очищающее действие.
Почему нельзя так называть стиральный порошок?
С химической точки зрения мы не можем так называть стиральный порошок. Если мы посмотрим на упаковку этих продуктов, то увидим, что там написано стиральные машины, а не стиральный порошок. Это правильно называть Стиральный порошок, так как его химический состав отличается от состава мыла.
Химический состав стирального порошка, а лучше сказать стирального порошка, основан на принципиальной разнице между мылом и моющим средством. См. Определение и химические характеристики этих материалов:
а) Моющие средства:
Это химические вещества с очень длинными цепями (большое количество углерода). состоит только из атомов углерода и водорода, формируя то, что мы называем областями неполярный. Кроме того, в конце этой длинной цепочки находится полярная группа.
Полярная часть моющего средства обусловлена наличием сульфонатной группы, то есть атома серы, взаимодействующего с три атома кислорода или фосфатная группа, в которой атом фосфора взаимодействует с тремя атомами кислород. Смотрите изображение структуры моющего средства:
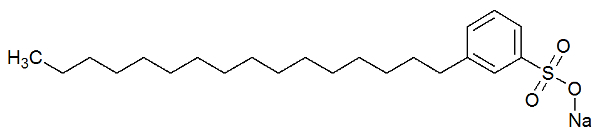
Структурная формула моющего средства
Полярная часть (образованная сульфонатом натрия) моющего средства способна взаимодействовать с молекулами воды. Неполярная часть (образованная только атомами углерода и водорода) взаимодействует с молекулами жира. Таким образом, моющее средство заставляет жир взаимодействовать с водой и образовывать эмульсию.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
б) Мыло
Это соли карбоновые кислоты возникла в результате химической реакции между жирами и сильными основаниями, такими как NaOH. См. Изображение химической структуры мыла:
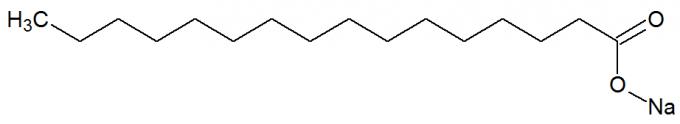
Структурная формула мыла
У них также есть длинные углеродные цепочки с неполярной и полярной частью. Таким образом, неполярная часть (состоящая только из атомов углерода и водорода) мыла может взаимодействовать с жиры и их полярная часть (образованная группой COONa) с водой образует эмульсии, например, моющие средства.
Поскольку в центре внимания этого текста находится химия «мыльного» порошка.или, точнее, химический состав порошкового моющего средства, мы представляем все химические вещества, входящие в его состав, а также важность каждого из них:
Химический состав порошкового моющего средства
анионное поверхностно-активное вещество (например, алкилбензолсульфонат натрия и сульфонат простого алкилового эфира натрия). Они связываются как с молекулой жира, так и с молекулой воды, таким образом удаляя жир из ткани;
Ферменты: Липазы и протеазы используются для удаления пятен. Это связано с тем, что с химической точки зрения ферменты являются биохимическими катализаторами, которые способствуют превращению сложных молекул в более простые. Таким образом, более мелкие молекулы легче удаляются с одежды;
Отбеливатель (перборат натрия): Он действует путем окисления, восстановления или ферментативного действия. В воде он производит перекись водорода, которая является мощным окислителем. Они химически реагируют с пигментом одежды, изменяя структуру и вызывая изменение цвета;
Оптические блокаторы: это вещества, которые поглощают ультрафиолетовое излучение или ультрафиолетовый свет и вскоре после этого излучают синий флуоресцентный свет, маскируя, например, желтоватый цвет одежды;
Ароматы: Это эссенции, которые оставляют на одежде приятный запах после стирки. Примечательно, что ароматизаторы - это эссенции (они относятся к эфирной функции);
Красители: Вещества, используемые для окрашивания продукта;
Секвестрирующие и хелатирующие агенты: ЭДТА (этилендиаминтетрауксусная кислота) является примером секвестранта. Они взаимодействуют с ионами кальция, магния и железа, присутствующими в основном в жесткой воде, не допуская взаимодействия каких-либо компонентов очищающего действия, таких как поверхностно-активное вещество.
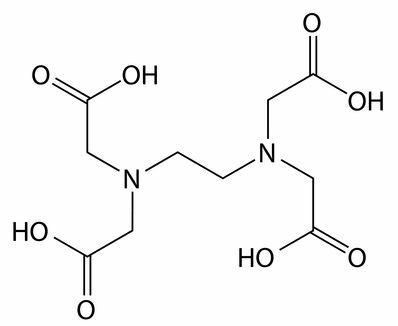
Структурная формула секвестранта ЭДТА
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Химия порошкового мыла»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/quimica-sabao-po.htm. Доступ 28 июня 2021 г.



