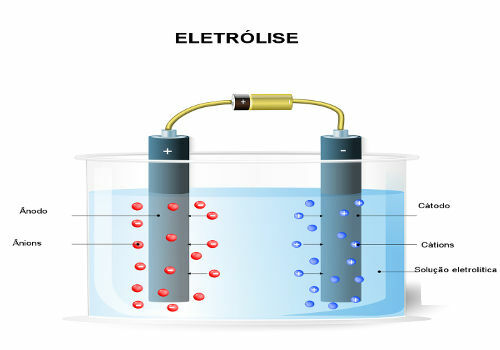
Каждая ячейка - это устройство, в котором происходит спонтанная окислительно-восстановительная реакция, генерирующая электрический ток, который, в свою очередь, используется для работы некоторого оборудования.
Свое название эти устройства получили потому, что первую батарею изобрел Алессандро. Еще в 1800 году он был образован дисками из цинка и меди, разделенными хлопком, пропитанным водой. рассол. Этот набор был помещен один поверх другого, нагромождение диски и образуют большую колонну. Каким был аккумулятор дисков, стали называться этим именем.

Батареи всегда состоят из двух электродов и электролита.. Положительный электрод называется катод и вот где реакция снижение. Отрицательный электрод - это анод и вот где реакция окисление. Электролит еще называют соляной мост и - ионопроводящий раствор.
Чтобы вы поняли, как при этом генерируется электрический ток, посмотрите на один из первых аккумуляторов, Куча Даниэля, в котором находилась емкость с раствором медного купороса (CuSO4 (водн.)) и, погруженная в этот раствор, была медная пластина. В другой отдельной емкости находился раствор сульфата цинка (ZnSO
4 (водн.)) и окунутую цинковую пластину. Два раствора были соединены солевым мостиком, который представлял собой стеклянную трубку с раствором сульфата калия (K2ТОЛЬКО4 (водн.)) со стекловатой на концах. Наконец, две пластины были соединены внешней цепью с лампой, свечение которой указывало бы на прохождение электрического тока: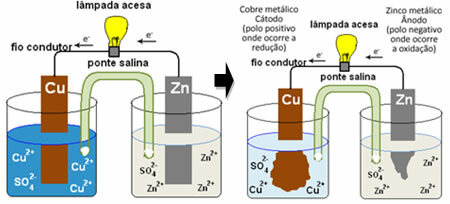
Что происходит, так это то, что цинк имеет большую тенденцию к окислению, то есть к потере электронов, поэтому металлический цинк лезвия работает как отрицательный электрод, анод, где происходит окисление: Zn(s) ↔ Zn2+(здесь) + 2 и-. Электроны, потерянные цинком, переносятся внешней цепью в медь, генерируя электрический ток, который включает лампу. Ионы меди в растворе получают электроны (восстанавливаются) и превращаются в металлическую медь, которая осаждается на медном листе. Это означает, что это положительный электрод, катод, где происходит восстановление: Жопа2+(здесь) + 2 и- ↔ задница(s).
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Сегодняшние батареи имеют тот же принцип работы, при котором один металл отдает электроны другому через проводящий раствор, и возникает электрический ток. Разница в том, что используемые сегодня батареи сухие, потому что в них не используется жидкий раствор в качестве электролита, как это происходит в батареях Даниэля.
Сегодня в продаже имеется очень широкий спектр батарей. Среди них наиболее распространены кислотные клетки (от Leclanché) ищелочные батареи.
Оба имеют цинк в качестве отрицательного электрода; с другой стороны, в качестве положительного полюса в середине сваи установлен графитовый стержень, окруженный диоксидом марганца (MnO2), древесный уголь (C) и влажную пасту. Разница в том, что в куче кислоты во влажной пасте используется хлорид аммония (NH).4Cl) и хлорид цинка (ZnCl2) - кислые соли - помимо воды (H2О). В щелочной батарее используется гидроксид калия (КОН), который является основанием.

Батареи Leclanché лучше всего подходят для оборудования, которое требует легкой и непрерывной разрядки, такого как пульт дистанционного управления, настенные часы, портативное радио и игрушки. С другой стороны, щелочные батареи имеют на 50-100% больше энергии, чем обычные батареи того же размера, что рекомендуется для оборудования, которое требуются более быстрые и интенсивные загрузки, такие как радиоприемники, CD / DVD-плееры, портативные MP3-плееры, фонарики, цифровые фотоаппараты и т.п.

Узнайте больше о том, какие электролиты и электроды используются в этих и других типах аккумуляторов. относительно того, какие типы оборудования они наиболее рекомендуются, читайте статьи по теме. ниже.
Дженнифер Фогача
Окончила химический факультет