Когда мы готовим еду у себя дома, мы используем газ для приготовления пищи. Одна из вещей, которые мы можем видеть в пламени, возникшем в результате сгорания этого газа, - это то, что его цвет обычно очень светло-голубой. Однако в большинстве реакций горения, таких как горение свечи, пламя желтое.

Тогда возникает вопрос:
«Если каждый пожар является результатом реакции горения, почему некоторые языки пламени имеют разные цвета?»
Чтобы понять, как это происходит, мы должны понять, что такое реакция горения и какие вещества присутствуют в каждой из упомянутых реакций.
Реакция горения происходит, когда топливо (окисляемый материал) потребляется окислителем (газообразным материалом, содержащим кислород) для выработки тепловой энергии (тепла).
Еще один важный момент, который нам необходимо знать о реакциях горения, - это то, что они могут происходить в полный или неполный. Если кислорода достаточно для потребления топлива, реакция завершится с образованием углекислого газа (CO2) и вода (H2О). В противном случае сгорание будет частичным, неполным с образованием окиси углерода (CO) и воды; или углерод (C) и вода.
В обоих рассматриваемых нами случаях окислителем является кислород, присутствующий в воздухе. Однако виды топлива разные. Варочный газ - это фактически сжиженный нефтяной газ (LPG), который представляет собой смесь углеводородов (алканов), основным топливом является бутан (C4ЧАС10). Таким образом, газ для приготовления пищи состоит из молекул алканов, которые имеют только три или четыре атома углерода, поэтому для его полного сгорания требуется мало кислорода.. Эту реакцию можно выразить следующим образом:
1С4ЧАС10 (г) + 13/2 O2 (г) → 4 СО2 (г) + 5 часов2О(грамм), ∆H <0
Не останавливайся сейчас... После рекламы есть еще кое-что;)
В случае свечей парафин является топливом для реакции, и он состоит из смеси алканов с атомами углерода, которые диапазон от 20 до 36. Тем самым, требуется намного больше кислорода, чтобы эта реакция протекала полностью. См. Пример:
1С24ЧАС50 (т) + 70/2 O2 (г) → 25 СО2 (г) + 25 часов2О(грамм), ∆H <0
В воздухе недостаточно кислорода для полного сгорания, поэтому оно происходит не полностью, как показано ниже:
1С24ЧАС50 (т) +49/2 O2 (г) → 24 СО(грамм) + 25 часов2О(грамм), ∆H <0
1С24ЧАС50 (т) +25/2 O2 (г) → 24С(s) + 25 часов2О(грамм), ∆H <0
Неполные реакции производят меньше энергии, чем полное сгорание. Это объясняет разницу между цветами пламени, поскольку желтое пламя, характерное для неполного сгорания, имеет меньшую энергию. Голубое пламя характерно для полного сгорания с большей энергией.
Это также объясняет образование сажи пламенем свечи (на фото ниже), которая представляет собой углерод, который считается продуктом неполного сгорания.
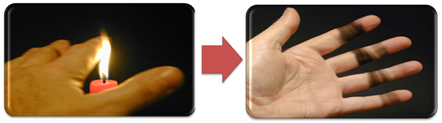
Но почему в горелке Бунзена может появиться желто-синее пламя, когда топливо не меняется?
В случае горелки Бунзена это достигается за счет регулирования подачи газа и воздуха. Если окно закрыто, вызывая попадание небольшого количества воздуха, полученное пламя будет желтым, потому что в нем будет мало кислорода для полного сгорания. Если регулировка газовоздушной смеси адекватная, мы получаем голубое пламя.
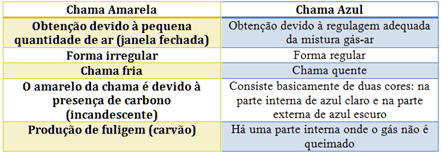
См. Характеристики каждого в таблице ниже:
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Горение и разноцветные языки пламени»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/combustao-chamas-cores-diferentes.htm. Доступ 28 июня 2021 г.
