Прежде чем говорить о номенклатуре четвертичная аммониевая соль правильно, важно помнить, что это за органическое соединение. Соль четвертичного аммония образуется в результате замены атомов водорода, присутствующих в катионе аммония (NH4+) на радикалы органический, как показано ниже:
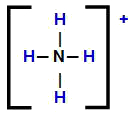
Структурная формула катиона аммония
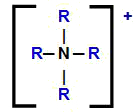
Структурная формула катиона аммония с заменой его атомов водорода на органические радикалы
В дополнение к замене атомов водорода каждая соль четвертичного аммония имеет любой анион, который сопровождает катион, полученный из аммония. Таким образом, мы можем представить общую структурную формулу этого соединения следующим образом:
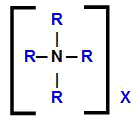
Общая структурная формула четвертичной аммониевой соли
Таким образом, очевидно, что в формуле четвертичной аммониевой соли присутствуют четыре одинаковых или разных органических радикала и любой анион (X). Чтобы провести номенклатуру этих соединений, мы должны принять это во внимание.
Посмотрите, как номенклатура четвертичной аммониевой соли по данным IUPAC (Международный союз теоретической и прикладной химии):
Название аниона + де + название радикалов в алфавитном порядке + аммоний
Теперь следуйте за некоторыми Примеры применения правила Номенклатура четвертичных аммониевых солей:
Бензил-октадецил-диметиламмоний йодид
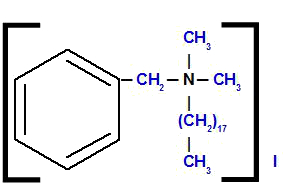
Анализируя структуру, мы видим, что анион в соединении присутствует я, который называется йодид. Слева от конструкции находится радикал бензил (соединение бензола с группой CH2). Сверху и справа у нас два радикала метил (CH3), который мы будем называть диметилом. Внизу радикальный октадецил, который имеет восемнадцать атомов углерода в своей цепи.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Таким образом, название начинается с йодида, за которым следует предлог, плюс название бензил, за которым следует октадецил (из-за алфавитного порядка) и, наконец, диметил с аммонием.
Наблюдение: Термины oct и di не участвуют в алфавитной последовательной организации составного имени.
тетраэтиламмоний хлорид
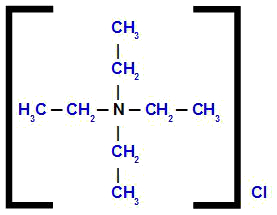
Анализируя структуру, мы видим, что анион в соединении присутствует Cl, который называется хлористый. В структуре присутствуют четыре органических радикала: этил (CH3-CH2-); поэтому они получили название тетраэтил.
Таким образом, название начинается с хлорида, за которым следует предлог, плюс название тетраэтил, за которым следует термин аммоний.
Бензил-тридецил-диметиламмоний бромид

Анализируя структуру, мы видим, что анион в соединении присутствует br, который называется бромид. Слева от конструкции находится радикал бензил (соединение бензола с группой CH2). Сверху и справа у нас два радикала метил (CH3), который мы будем называть диметилом. Внизу радикальный Tridecil, так как в его цепи тринадцать атомов углерода.
Таким образом, название начинается с йодида, за которым следует предлог, плюс название бензил, за которым следует тридецил (из-за алфавитного порядка) и, наконец, диметил с аммонием.
Дифенил-диметиламмоний сульфат
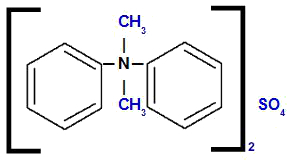
Анализируя структуру, мы видим, что анион в соединении присутствует ТОЛЬКО4, который называется сульфат. Слева и справа от структуры у нас есть фенильный радикал (бензол), который будет называться «дифенил». Вверху и внизу у нас есть метильные радикалы (CH3), который мы будем называть диметилом.
Таким образом, название начинается с сульфата, за которым следует предлог, плюс название дифенил, за которым следует диметил (из-за алфавитного порядка) и, наконец, аммоний.
Автор: Диого Лопес Диас