Межмолекулярные силы отвечают за удержание молекул вместе при образовании различных соединений, они классифицируются как:
Сила, индуцированная диполем: она вызвана накоплением электронов в определенной области молекулы.
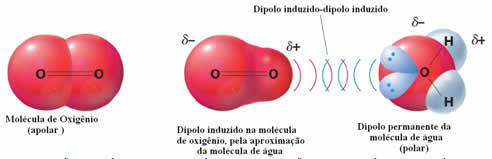
Межмолекулярные взаимодействия, присутствующие в неполярных молекулах, являются дипольными, но они не происходят постоянно, распределение электронов в электросфере этих молекул однородно. Однако в какой-то момент на концах происходит скопление зарядов δ + и δ - (полюсов), именно здесь силы появляются индуцированные диполи, и, как следует из названия, они побуждают соседние молекулы также вступать в дисбаланс.
См. Примеры неполярных соединений, молекулы которых взаимодействуют посредством дипольных сил:
Cl2, CO2, CH4, H2, O2
Диполь-дипольные силы: межмолекулярные силы, присутствующие в полярных соединениях.
δ + δ- δ + δ- δ + δ-
ЧАС? Br H? Br H? br
Обратите внимание, что в молекулах бромистоводородной кислоты (HBr) есть полюса δ + а также δ-, они ответственны за полярность этой молекулы.
Примеры полярных соединений, в которых происходит диполь-дипольное взаимодействие:
ЧАС2S, CO, SO2, HCl
Водородные связи: это самое сильное взаимодействие, которое происходит между молекулами, по сравнению с гораздо более сильной диполь-дипольной силой. Эта связь возникает между молекулами, которые содержат атомы водорода, связанные с атомами азота, фтор, кислород, то есть очень электроотрицательные элементы, поэтому полюса δ + и δ- больше акцентировано.
Молекула воды является классическим примером водородных связей, когда атомы H плотно связываются с атомами H других молекул, образуя H-цепь.20.
Посмотрите, какая межмолекулярная сила более интенсивна, на рисунке ниже:

Стрелка указывает возрастающий порядок интенсивности взаимодействия.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Лирия Алвес
Окончила химический факультет
Бразильская школьная команда
Узнать больше:
Межмолекулярные силы и растворимость
Эксперимент, позволяющий проверить, какое вещество полярное, а какое неполярное.
Общая химия - Химия - Бразильская школа
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Типы межмолекулярных сил»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/tipos-forcas-intermoleculares.htm. Доступ 27 июня 2021 г.
Химия

Перейдите по этой ссылке и узнайте об органической функции фенолов, группы кислородсодержащих веществ, от высокая реакционная способность, кислотность которых выше, чем у спиртов (соединений, которые также имеют группу гидроксил). Его структура отличается наличием гидроксидной группы (ОН), непосредственно связанной с ароматическим соединением.